Источник: Biomimetics
DOI: https://doi.org/10.3390/biomimetics11020128
Авторы: Mansoureh Rezapourian, Anooshe Sadat Mirhakimi, Mahan Nematollahi, Tatevik Minasyan, Irina Hussainova
Перевод с английского
Первая часть тут
Аннотация
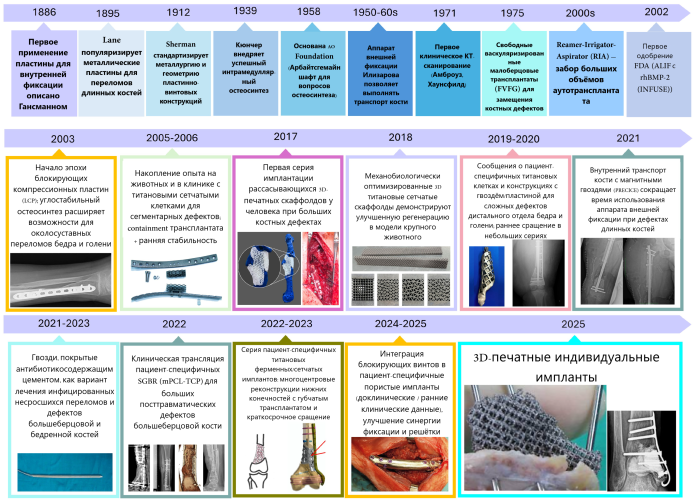
2. Историческая эволюция имплантации решетчатых протезов с планированием на основе КТ.
От Илизарова до АМ: эволюция методов лечения дефектов бедренной и большеберцовой костей.
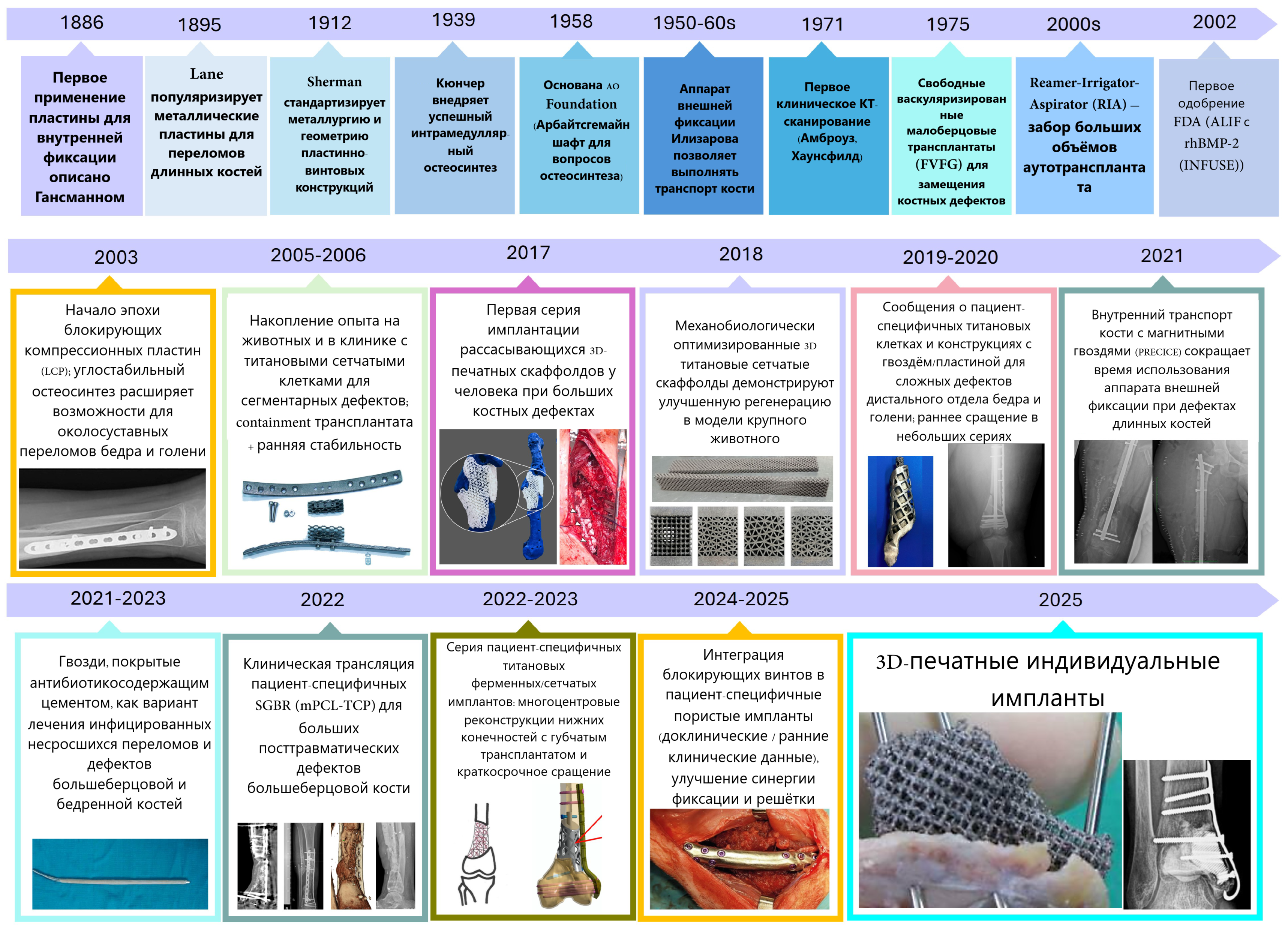
3. Процесс персонализации и обработки изображений
| Год, Ref [n] | Рабочий процесс «Изображение → Модель» (КТ/μКТ; ключевые шаги) |
| 2013, [1] | КТ стандартизированного композитного бедра (4-е поколение, большое левое Sawbones); матрица/пиксель/срез не указаны; сегментация не указана; КТ-картирование HU из композитной кости. |
| 2014, [70] | Нет конвейера КТ-модели пациента; настольная μКТ имплантатов SLM Ti (пороги 77–255/85–255/96–255); расчёт пористости, размеров пор и стержней; без сегментации DICOM/зеркалирования; без КТ-CAD. |
| 2015, [65] | Без КТ (стандартизированное композитное бедро 3-го поколения); сегментация N/A; геометрия использована напрямую (без зеркалирования); канал подготовлен сверлением/рассверливанием через булевы операции; КТ-картирование HU не использовалось. |
| 2018, [68] | КТ-дизайн, матрица/пиксель/толщина среза НУ; CAD создан из 3D-КТ производителем (DePuy Synthes); зеркалирование не указано; рентген и КТ для наблюдения. |
| 2018, [67] | КТ (здоровое взрослое бедро, DICOM), сегментация в Mimics (пороговая обработка ROI, заживление дефектов, шумоподавление); экспорт в SolidWorks, HU-картирование для пористости и модуля упругости. |
| 2019, [15] | Без КТ/DICOM (CAD композитного бедра от производителя), оптическое 3D-сканирование белым светом, сборка в SolidWorks; сегментация N/A. |
| 2019, [5] | КТ (среднестатистическое бедро), 3D-реконструкция в Mimics → Geomagic Studio; булевы операции с элементарными ячейками; экспорт в CAD. |
| 2019, [69] | КТ (середина диафиза бедра), экспорт DICOM, сегментация и 3D-реконструкция в Mimics, экспорт STL. |
| 2019, [2] | Высокоточная КТ конструкции PMMA-спейсера для виртуального хирургического планирования; зеркалирование контралатеральной конечности; данные отправлены производителю для CAD/3D-печати. |
| 2020, [9] | In vivo и ex vivo μКТ (Skyscan 1176); реконструкция в CTAn и Simpleware ScanIP; количественный анализ с пороговыми значениями. |
| 2020, [3] | КТ (двусторонние бедра), создание 3D-моделей в Creo Parametric, зеркалирование интактного бедра для восстановления повреждённого. |
| 2021, [14] | КТ (здоровое бедро), 512×512, пиксель 0.6445 мм, срез 1 мм; сегментация в Mimics v17; HU–плотность–E картирование; экспорт в ANSYS и STL. |
| 2021, [6] | In vivo рентгенография и μКТ у крыс; оценка пористости и морфологии скаффолдов. |
| 2021, [64] | КТ → 3D Slicer → STL (Meshmixer); SLA-печать для валидации. |
| 2021, [4] | КТ + μКТ (Inveon); сегментация в Mimics; порог HU 1000-3885; анализ peri-implant и intraporous зон. |
| 2022, [7] | КТ/DICOM, MIMICS 18.0 (230–1883 HU), создание сегментарного дефекта в SpaceClaim. |
| 2022, [11] | КТ пациента (остеосаркома), дефект определён анатомически (без зеркалирования). |
| 2023, [62] | КТ, Mimics 21.0 + Magics 22.0; зеркалирование контралатеральной стороны; остеотомия 90 мм. |
| 2023, [8] | μКТ напечатанного скаффолда (Scanco μCT 100) для верификации геометрии (без модели пациента). |
| 2023, [17] | КТ, 1816 срезов, сегментация в Mimics 10.01, экспорт STL, нарезка в Cura. |
| 2023, [10] | КТ овечьей плюсневой кости, InVesalius; шаблонирование дефекта 13 мм. |
| 2023, [13] | Ex vivo XCT explanted имплантатов; ML-сегментация (Ilastik + U-Net). |
| 2024, [16] | КТ кроличьей большеберцовой кости, Meshmixer + Geomagic → SolidWorks. |
| 2024, [66] | 2D рентгеновские снимки → алгоритмическая 3D-реконструкция → CAD модульных блоков BoneBricks. |
| 2024, [12] | КТ-модель (ENOVO-186), CAD в Creo Parametric. |
| 2025, [63] | КТ NIH Visible Human, сегментация в Amira–Avizo, HU–E картирование в ANSYS. |
| Сокращения: NR — Не указано BMD — минеральная плотность кости (МПК) CSA — площадь поперечного сечения CTAn — CT-Analyser (программа для анализа изображений микро-КТ) NIH — Национальные институты здравоохранения США ROI — область интереса SLA — стереолитография TV — общий объём ML — машинное обучение BII — контакт кость–имплантат BIC — интерфейс кость–имплантат | |
4. Решеточное моделирование и архитектура
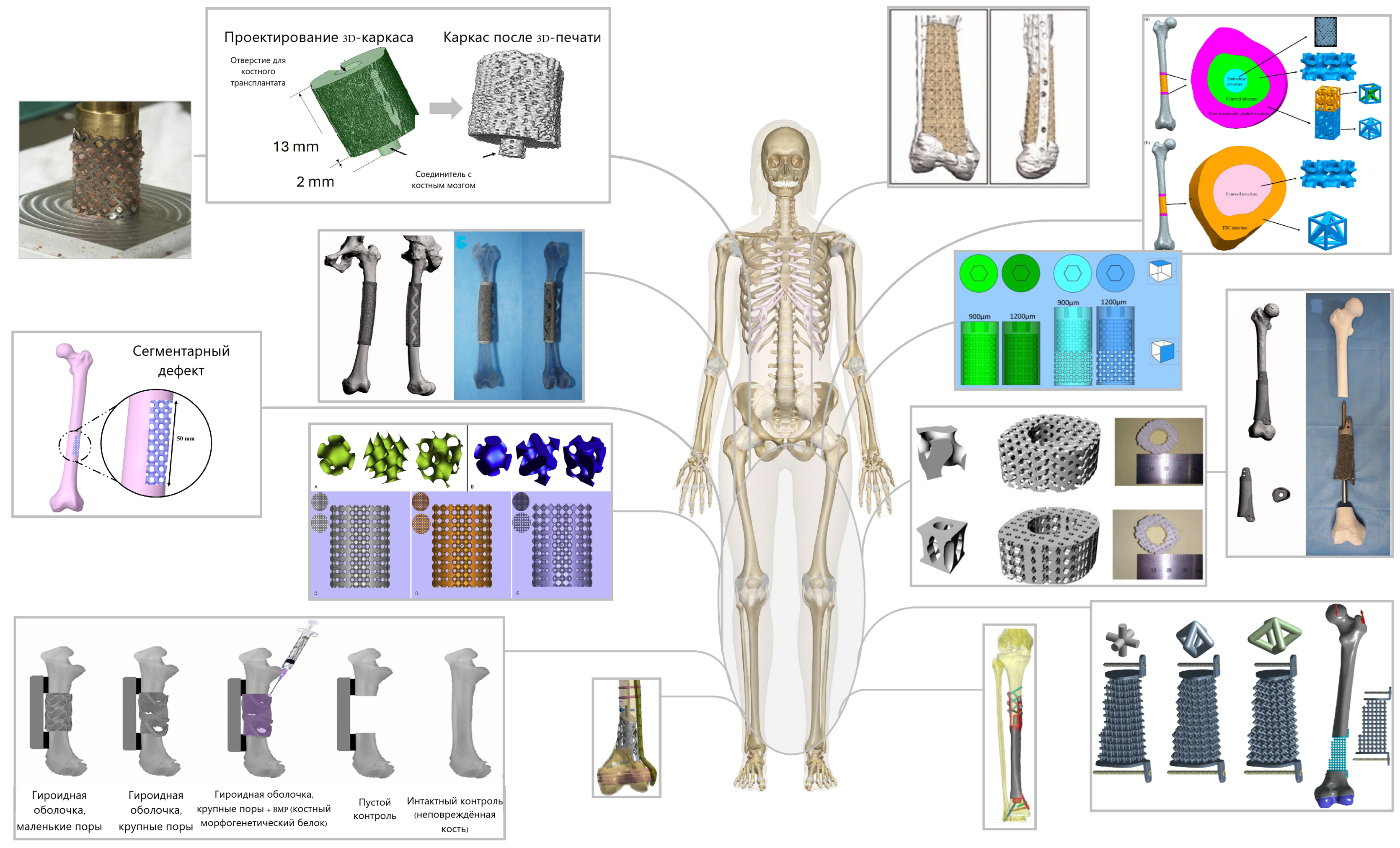
| Год, ссылка [n] | Тип решётки | Элементарная ячейка (мм; X×Y×Z) | T (мм) | Размер пор (мкм) | Отн. плотность/Пористость (%) | SA/VR (мм⁻¹) | Градиент (тип) | Драйвер градиента | Цели дизайна | CAD-программы |
| 2013, [1] | Стержневая (регулярная открытая ячеистая; цилиндрический скаффолд) | — | 0,3–0,8 | 800/1100/1500/1800 | 61–81 (эфф.); 64–93 (скафф.) | — | Отсутствует (постоянная ОП) | Параметрический перебор по правилам | Соответствие модулю упругости; снижение экранирования напряжений; минимизация зазора; σvM < 660 МПа | NR |
| 2014, [70] | Стержневая (додекаэдрическая ячейка) | 0,5 × 0,5 × 0,5 | 0,12/0,17/0,23 | 500 (номин.); ≈560–610 (μКТ) | 84/78/68 | NR | Отсутствует (три группы жёсткости) | — | Изменение жёсткости импланта для изучения передачи нагрузки | NR |
| 2018, [68] | Стержневая сотовая титановая сетка | Цилиндр Ø20 × 40 мм, центральный канал Ø10 мм | 1,2/1,6 | NR (макроканалы) | NR | NR | Отсутствует | N/A | Механобиологическая оптимизация жёсткости для снижения экранирования напряжений и стимуляции регенерации | Собственное ПО производителя (DePuy Synthes) |
| 2018, [67] | Стержневая (кубооктаэдр, гексаэдр и др.) | NR (на основе куба) | NR | NR | 5–60 | NR | Градиент относительной плотности | По правилам (PS:BT) | Соответствие модулю упругости, снижение SS, открытая структура | Mimics, SolidWorks, Creo |
| 2019, [15] | Стержневая (ортогональная сетка) | NR | NR | NR | 60–70 | NR | Отсутствует | N/A | Соответствие эффективному модулю и энергии деформации | SolidWorks 2016 |
| 2019, [5] | Сферические поры; TPMS-гироид; топологически оптимизированная | 2,4 × 2,4 × 2,4 | NR | 1110 (SP) | 70 | NR | Отсутствует | N/A | Максимизация механических свойств при 70% пористости | Mimics + Geomagic Studio |
| 2019, [69] | Сотовая (квадратные/треугольные поры) | 32 × 25,5 × 13,5 | 0,2032 | 1250 | ≈68–83 | NR | Отсутствует | N/A | Создание скаффолдов с жёсткостью кортикальной кости | CATIA + Insight |
| 2019, [2] | Пациент-специфичная ферменная титановая клетка | Анатомическая под дефект | NR | NR | Высокопористая | NR | Отсутствует | N/A | Реконструкция по Masquelet с большим объёмом трансплантата | ПО производителя |
| 2020, [9] | TPMS-гироид + гибрид с оболочкой | 0,81 | 0,18–0,23 (оболочка) | 430 | 60 / 43 | NR | Гибрид оболочка+решётка | По правилам | Подгонка под дефект крысы, улучшение прочности | ScanIP |
| 2020, [3] | Сетка + сплошная оболочка | 10×10, толщина 1,5 мм | 1,5 | NR | NR | NR | Отсутствует | По правилам | Лёгкость, снижение SS, остеоинтеграция | Creo Parametric v5.0 |
| 2021, [14] | Стержневая (кубическая) | NR | ≥0,5 | NR | Переменная | NR | Градиент плотности/толщины стенок | По КТ (HU–E) | Соответствие модулю, снижение SS | Mimics 17 |
| 2021, [6] | TPMS-гироид (листовой) | 3×3×3 и 6×6×6 | 0,30 / 0,60 | 739 / 1076 | CAD 70; μКТ 62,8–70,8 | NR | Отсутствует | — | Врастание кости, стабильность интерфейса | NR |
| 2021, [64] | TPMS (разные) + стержневые + соты | 20×20×20 | NR | NR | NR | NR | Отсутствует | — | Сравнение механических свойств | Rhino 7 |
| 2021, [4] | Пористый Ti6Al4V | NR | 0,24–0,32 | 400–600 | 60–80 | NR | Отсутствует | N/A | Одноэтапная реконструкция без трансплантата | Mimics Research 20.0 |
| 2022, [11] | Поверхностная решётка + отверстия | 5×5 / 10×10 | 2 | 5000 | N/A | NR | Отсутствует | Масштабирование под пациента | Минимизация SS, заполнение трансплантатом | Geomagic + Creo |
| 2023, [62] | Гибрид (стержневая + имитация трабекул) | NR | NR | NR | 55 / 65 / 86 | NR | Градиент морфологии и пористости | По регионам | Увеличение деформации на интерфейсе, снижение SS | Mimics 21, Magics 22 |
| 2023, [8] | Стержневая открыто-пористая (ATS-блоки) | 8×8×5,8 | 0,2–0,5 | 400–800 | 50–62 % | NR | Отсутствует (дискретные варианты) | N/A | Модульная LEGO-сборка под пациента | Fusion 360 + Magics |
| 2023, [17] | Без решётки (сплошная модель) | — | — | — | 100% | NR | Отсутствует | N/A | Создание модели бедра из CF-PEEK для тестов | Mimics + SOLIDWORKS |
| 2023, [10] | Робокастинговая стержневая биокерамика | Индивидуальная под дефект 15 мм | — | 360,8 | 59,3 / ≈40,7 | ≈5,77 | Отсутствует | N/A | Оптимизация пористости и поверхности | InVesalius |
| 2023, [13] | Стержневая кубооктаэдрическая (Ti–19Nb–14Zr) | 0,9 / 1,2 | NR | 350/450 | NR | NR | Отсутствует | N/A | Изучение врастания кости в зависимости от размера ячеек | NR |
| 2024, [16] | Гибрид (оболочка + решётка + HAp) | NR | NR | NR | 50–70 % (радиальный) | NR | Градиент плотности и материала | По правилам | Снижение SS, защита HAp | SolidWorks + Meshmixer |
| 2024, [66] | Стержневая модульная («кирпичики кости») | NR | NR | NR | Переменная | NR | Градиент пористости (модули) | Анатомически-driven | Быстрая модульная сборка | Собственный алгоритм |
| 2024, [12] | Стержневая кубооктаэдрическая | 2×2×2 | 0,6–1,0 | NR | Переменная | NR | Отсутствует | По результатам FE | Целевая деформация интерфейса ~4000 μϵ | ANSYS Workbench (Material Designer) |
| 2025, [63] | Стержневая (стоечная) | 6×6×6 | 1,5 / 2,0 / 2,5 | NR | NR | NR | Отсутствует | Перебор параметров | Снижение SS, соответствие деформации intact кости | ANSYS DesignModeler |
Материалы и производство
| Год, Ref [n] | Исходный материал | Метод изготовления | Оборудование/компания | Основные параметры процесса | Пост‑обработка | Финальное изделие/участок кости | Методы характеристизации |
| 2013, table3.html | Ti6Al4V | SEBM | – | – | – | Непористые образцы для растяжения и изготовленные на заказ открыто‑пористые образцы для испытаний на сжатие | – |
| 2014 | Ti6Al4V ELI grade 23, 25–45 μm | SLM | Layerwise NV (Leuven, Belgium) | Yb:YAG волоконный лазер; Ti‑подложка; LP = 42 W; LT = 30 μm; ν = 260 mm/s | EDM | Высокопористые Ti‑импланты для сегментного костного дефекта; тип элементарной ячейки: додекаэдр; размеры стоек = 120, 170, 230 μm; размер пор = 500 μm | – |
| 2018 | Ti‑сплав | Лазерное спекание | Изготовлено компанией DePuy Synthes (Warsaw, IN, USA) | – | – | Ti‑сетчатые каркасы | BSE‑SEM для исследования образования кости внутри каркаса |
| 2019 | Фотополимер VeroWhitePlus (RGD835) (жидкая смола) | Струйное нанесение материала (PolyJet) | 3D‑принтер PolyJet, Objet Eden260VS (Stratasys, Minnetonka, MN, USA) | Разрешение по слою 16 μm | – | Прямоугольные и цилиндрические каркасы с квадратным и шестигранным рисунком и пористостью 60–70% | DIC |
| 2019, intechopen | Композитный шликер PLA–β‑TCP‑HA (соотношение 2:1:1) | Экструзионная биопечать | Биопринтер (Regenovo Biotechnology Corp., Hangzhou, China) | Скорость печати 0.20 mm/min; P = 0.25 MPa; T = 25 °C; ⌀ печатающей иглы = 610 μm | – | Биокомпозитные каркасы со сферической порой, архитектурой gyroid и топологической архитектурой | SEM‑анализ для оценки внешнего вида образцов до и после деградации |
| 2019 | ABS‑полимер | FDM | 3D‑принтер Fortus360mc (Stratasys, Minnetonka, MN, USA) | Сопло T10; L<sub>Tmin</sub> = 0.127 mm; четыре варианта укладки растров; минимальная толщина слоя = 0.127 mm; ширина растров = 0.2032 mm; максимальный воздушный зазор между дорожками = 1.27 mm | Удаление опорной структуры из водорастворимого материала SR30 | Каркас для сегмента бедренной кости | Оценка пористости методом единичного куба и методом относительной плотности |
| 2019, ijmmm.ustb | Ti6Al4V | Наиболее вероятно EBM (изготовлено 4Web Medical; Frisco, TX, USA) | EBM‑установка (Arcam AB, Mölndal, Sweden) | – | – | Индивидуальные 3D‑печатные титановые кейджи | – |
| 2020, pmc.ncbi.nlm.nih | HA‑порошок, преобразованный в шликер, пригодный для 3D‑печати | Косвенное AM: струйное нанесение материала (Inkjet DoD) для восковых форм и последующей пропитки шликером | 3Z Studio (Solidscape, Multistation, Saint-Malo, France); регулируемый LT = 6, 12, 19, 25 μm) | LT = 25 μm; ориентация печати вертикальная (длина импланта вдоль оси Z принтера); равномерное увеличение начальной CAD‑модели на 14% для компенсации усадки при спекании | Сушка при RT в течение ночи; выжиг связующего при 500 °C; спекание на воздухе при 1200 °C со скоростью нагрева 4 °C/min в течение 2 h | HA‑импланты с пористостью типа gyroid, усиленные наружной оболочкой, подобной кортикальной кости | Программа ImageJ (freeware, National Institutes of Health, Bethesda, MD, USA) для анализа пористости (форма и размер микропор); SEM для анализа макротопографии поверхности; FTIR и XRD для анализа фазовой стабильности исходного HA |
| 2020, scribd | Ti‑сплав (~30 μm размер частиц) | LPBF | AM400 (Renishaw, Wotton-under-Edge, Gloucestershire, UK) | – | Поверхность напечатанного импланта обработана дробеструйно, далее применён специфический протокол очистки | Индивидуальный 3D‑печатный тitanовый имплант | – |
| 2021 | Ti6Al4V; (4–40 μm размер частиц) | DMLS | EOSINT M280 (EOS GmbH, Krailling, Germany) | Yb‑волоконный лазер; диаметр пятна = 80 μm; ν = 1200 mm/s; HD = 0.14 mm | Снятие напряжений термообработкой при 800 °C в течение 1.5 h в камере с Ar | Пористый имплант Ti6Al4V для областей большого вертела, диафиза и мыщелков | – |
| 2021, scribd | Ti6Al4V (медицинский класс) | LPBF | 3D Systems DMP ProX 320 (Rock Hill, SC, USA) | – | HIP для снижения остаточных напряжений и улучшения пластичности; EDM; микродробеструйная обработка | Решётчатая структура топологии gyroid‑sheet с пористостью 70% и средним размером пор 740 или 1100 μm | ImageJ (NIH) и плагин BoneJ для измерения размера пор и толщины стенок |
| 2021 | (1) биоразлагаемая смола на основе соевого масла; (2) биоразлагаемая УФ‑отверждаемая смола с 5% HA и 5% CPP | SLA | SLA‑3D‑принтер (Anycubic Photon, Shenzhen, China) | – | Образцы нагревались 40 h при 230 °C перед испытаниями на растяжение | Каркасы TPMS и FGLS с размером пор 100–500 μm | Метод вытеснения (погружение) для анализа пористости и плотности |
| 2021, sciencedirect | Ti6Al4V | EBM | EBM S12 система (Arcam AB, Mölndal, Sweden) | – | Обработка воздушной струёй и ультразвуковая очистка | Пористые импланты Ti6Al4V с размером пор 40–600 μm, диаметром стоек 240–320 μm и пористостью 60–80% | – |
| 2022, rcog | Ti6Al4V | LPBF | AM400 (Renishaw, Wotton-under-Edge, Gloucestershire, UK) | – | – | Имплант‑каркас для костной ткани | – |
| 2023, pmc.ncbi.nlm.nih | Чистый титан (Ti grade II, d₅₀ = 41±2 μm) | SLM | SLM 250HL (SLM Solutions GmbH, Lübeck, Germany) | LT = 30 μm; внешний контур: LP = 100 W, ν = 550 mm/s; внутренний контур: LP = 175 μW, ν = 833 μmm/s | Один набор ATS с текстурированной поверхностью, обработанной двойным кислотным травлением при повышенной температуре в течение 15 min | ATS с дизайном, вдохновлённым LEGO®‑соединением, с поверхностями: исходная SLM и текстурированная (двойное кислотное травление) | Анализ впитывания (поглощение жидкости твёрдым каркасом); шероховатость поверхности лазерным профилометром |
| 2023 | Катушка филамента 3DXTECH CF‑PEEK | FDM | 3D‑принтер Pratham~5.0 (Make3D.in, Surat, India) | Один экструдер; ⌀ сопла поддерживающего экструдера = 400 μm; температура сопла экструдера = 300 °C; температура платформы = 120 °C; LT = 100–500 μm; время печати = 12 h | – | Модель бедренной кости | – |
| 2023, hal | Клинически проверенные чернила с 45 об.% HA | Экструзия материала (DIW) | Устройство роботизированного нанесения 3-D Inks (Stillwater, Tulsa, OK, USA) | – | Сушка при 400 °C в течение 1 h; спекание при 1300 °C в течение 2 h; стерилизация при высокой концентрации формальдегида при 60 °C и относительной влажности 75–100% | Каркас для 15 mm сегмента кости с пористостью 59.30%, удельной площадью поверхности 5768.91 m⁻¹ и размером пор 60.80 μm | – |
| 2023 | Ti-19Nb-14Zr (at%), ZTM14N | LPBF | SLM 125HL (SLM Solutions GmbH, Lübeck, Germany) | Yb‑волоконный лазер; LP = 200 W; LT = 30 μm; температура платформы = 200 °C | Очистка и стерилизация | Решётчатые импланты для большеберцовой и плюсневой костей с тремя цилиндрическими дизайнами и двумя основными размерами элементарной ячейки (900 и 1200 μm) и диагональными размерами ячейки (350 и 450 μm) | He‑пикнометрия для определения объёмной плотности и относительной плотности |
| 2024 | Ti6Al4V | SLM | EOSINT M280 (EOS GmbH, Krailling, Germany) | Yb‑волоконный лазер; L<sub>Pmax</sub> = 200 W | Испытывались режимы отжига: 723–923 K и 40–240 min; оптимальный режим: 842.8 K, 77.6 min | Каркас Ti6Al4V с радиальным градиентом пористости (50–70%), заполненный HA, для критического дефекта большеберцовой кости | Наноиндентирование для определения изменений механических свойств отожжённого каркаса, включая модуль упругости и твёрдость |
| 2024 | PCL‑филамент | FDM | Коммерчески доступный 3D‑принтер | Температура шприца = 65 °C; ⌀ сопла экструзии = 250 μm; стратегия сканирования «зигзаг» | Сборка модульных блоков каркаса хирургом | Структура каркаса для дистального дефекта кости 67.60 mm и модели бедренной кости | – |
| 2024 | Ti6Al4V | LPBF | AM250 (Renishaw plc, Wotton-under-Edge, Gloucestershire, UK) | Диаметр пятна = 75 μm; LT = 30 μm; LP = 100 W; ET = 60 μs; PD = 75 μm; HD = 20 μm | Комплементарная модель бедренной кости изготовлена методом FDM‑печати полимером | OLS с пористостью 69.8% и нелаттис‑структурированный сплошной имплант; элементарная ячейка решётки: кубоктаэдр | – |
HD — расстояние между штрихами; HIP — горячее изостатическое прессование; LT — толщина слоя; PD — расстояние между точками; RT — комнатная температура;
SEBM — селективное электронно-лучевое плавление; ν — скорость сканирования; YAG — иттрий-алюминиевый гранат.
5. Обзор методологии: имитационные, экспериментальные и клинические исследования.
5.1. Методы численного моделирования для сегментной реконструкции на основе решеток
| Год, Ref [n] | Материальная модель | Граничные условия/нагрузки | ПО/сетка | Выходные данные/метрики | Валидация | Ключевые механические выводы |
| 2013, [1] | Линейно‑упругая | Дистальный отдел бедра зафиксирован | Abaqus 6.10/C3D8 | Эквивалентные напряжения по Мизесу | Одноосные испытания пористого Ti | Большая жёсткость: меньшее перемещение |
| Изотропная кость | Нагрузка при стойке на одной ноге | Осевая жёсткость | Комплаентные дизайны: избыточная деформация | |||
| Однородный каркас (E из испытаний) | Межфрагментарное перемещение | Компромисс между пористостью и стабильностью | ||||
| 2015, [65] | Линейно‑упругая | Альтернативная дистальная фиксация | ADINA 8.9/NR | Жёсткость конструкции | Сравнение с данными литературы | Выбор BC существенно влияет на жёсткость |
| Изотропные кость и фиксаторы | Осевая, изгиб, кручение | Напряжения в штифтах и винтах | Упрощённые BC искажают передачу нагрузки | |||
| 2018, [68] | Линейно‑упругая | Осевая компрессия (1372 N) | NR | Эквивалентные напряжения по Мизесу | Выбор каркаса на основе FE‑анализа | Мягкий каркас: более высокая деформация мозоли |
| Изотропные Ti, кость, костная мозоль | Изгибающая нагрузка (86 N) | Главная деформация | Жёсткий каркас: экранирование напряжений | |||
| Распределение деформаций в порах | ||||||
| 2018, [67] | Линейно‑упругая | Дистальный отдел бедра зафиксирован | ANSYS/Hypermesh 2 mm tetra | Распределение напряжений | Нет (только численное моделирование) | Бóльшая пористость: меньшая жёсткость |
| Изотропные кость и каркас | Осевая компрессия | Глобальное перемещение | Повышенные напряжения в каркасе | |||
| 2019, [15] | Линейно‑упругий полимер | Компрессия до 500 N | Abaqus 6.13/NR | Эффективный модуль | Испытания на сжатие | Гомогенизированная модель совпадает с детализированной решёткой |
| Ортотропная гомогенизация | Поле деформаций по всему объёму | 3D DIC | Снижение вычислительных затрат | |||
| 2019, [5] | Линейно‑упругий композит | Одноосная компрессия | ANSYS/NR | Эквивалентные напряжения по Мизесу | Испытания на сжатие | Каркасы gyroid и TO более жёсткие, чем со сферическими порами |
| Изотропное поведение | Управление по перемещению | Эффективная жёсткость | ||||
| 2020, [3] | Линейно‑упругая кость | Дистальный отдел бедра зафиксирован | ANSYS/NR | Напряжения и деформации | Нет | Приемлемые напряжения на всех стадиях заживления |
| Ti‑имплант | Стойка на одной ноге | Смещение суставной поверхности | Пиковые напряжения сразу после операции | |||
| Зависимость от стадии заживления | ||||||
| 2021, [14] | Неоднородная кость на основе HU | Дистальное закрепление | ANSYS/NR | Жёсткость конструкции | Испытания на сжатие | Дизайны с согласованной жёсткостью уменьшают рассогласование |
| Линейно‑упругая | Физиологическая нагрузка | Деформация кости | ||||
| 2021, [4] | Линейно‑упругая | Трёхточечный изгиб | Abaqus 6.4/NR | Изгибная жёсткость | Ex vivo испытания на изгиб | Достаточная жёсткость |
| Изотропная кость | Напряжения на интерфейсе | Безопасные напряжения на интерфейсе | ||||
| 2022, [7] | Линейно‑упругая | Осевая компрессия | ANSYS/Hex mesh | Связь «напряжение–пористость» | Нет | TPMS восстанавливает передачу нагрузки |
| Изотропные каркас и кость | Стойка на одной ноге | Деформация | Снижение концентраций напряжений | |||
| 2022, [11] | Линейно‑упругая | Физиологическая нагрузка на сустав | ANSYS 19.0/NR | Напряжения и деформации | In vitro тензометрия | Снижение экранирования напряжений |
| Изотропные кость и Ti | Жёсткость конструкции | Сохранение жёсткости | ||||
| 2023, [62] | Линейно‑упругая | Дистальная фиксация | NR/NR | Напряжения | Нет | Градиенты снижают пиковые напряжения |
| Каркас с градиентом жёсткости | Нагрузки повседневной активности | Микроперемещения на интерфейсе | Меньшие микроперемещения | |||
| 2023, [8] | Линейно‑упругий Ti | Распределённое давление | NX 12.0/Tetra | Напряжения | Испытания на сжатие | Большой запас до начала текучести |
| Изотропный | Фиксированная противоположная грань | Деформация | ||||
| 2023, [17] | Линейно‑упругая | Бедренная кость зафиксирована | ANSYS/5 mm mesh | Напряжения | Испытания на сжатие | CF‑PEEK даёт отклик, наиболее близкий к бедренной кости |
| Кость, PEEK, CF‑PEEK | Нагрузка приложена к головке бедренной кости | Деформация | ||||
| 2024, [16] | Линейно‑упругая | Нагрузка на плато большеберцовой кости | ANSYS/NR | Распределение напряжений | Наноиндентирование | Градиентная пористость снижает пиковые напряжения |
| Свойства по правилу смесей | Напряжения в каркасе | Испытания на сжатие | ||||
| 2024, [12] | Линейно‑упругая кость | Дистальная фиксация | ANSYS/Tetra | Деформация кости | Сравнение с тензометрическими измерениями | 0.8 mm/45° даёт оптимальный баланс |
| Ортотропная решётка | Нагрузка 2800 N | Напряжения в решётке | ||||
| 2025, [63] | Линейно‑упругая | Дистальный отдел бедра зафиксирован | ANSYS/NR | Напряжения | Нет | Pillar‑решётка снижает напряжения |
| Изотропные материалы | Стойка на одной ноге | Перемещения | Уменьшается смещение суставной поверхности |
ATS — сборный титановый каркас; DIW — прямая печать чернилами; EDM — электроэрозионный станок; ET — время экспозиции; HD — расстояние между штрихами; HIP — горячее изостатическое прессование; LT — толщина слоя; PD — расстояние между точками; RT — комнатная температура; SEBM — селективное плавление электронным пучком; ν — скорость сканирования; YAG — иттрий-алюминиевый гранат.
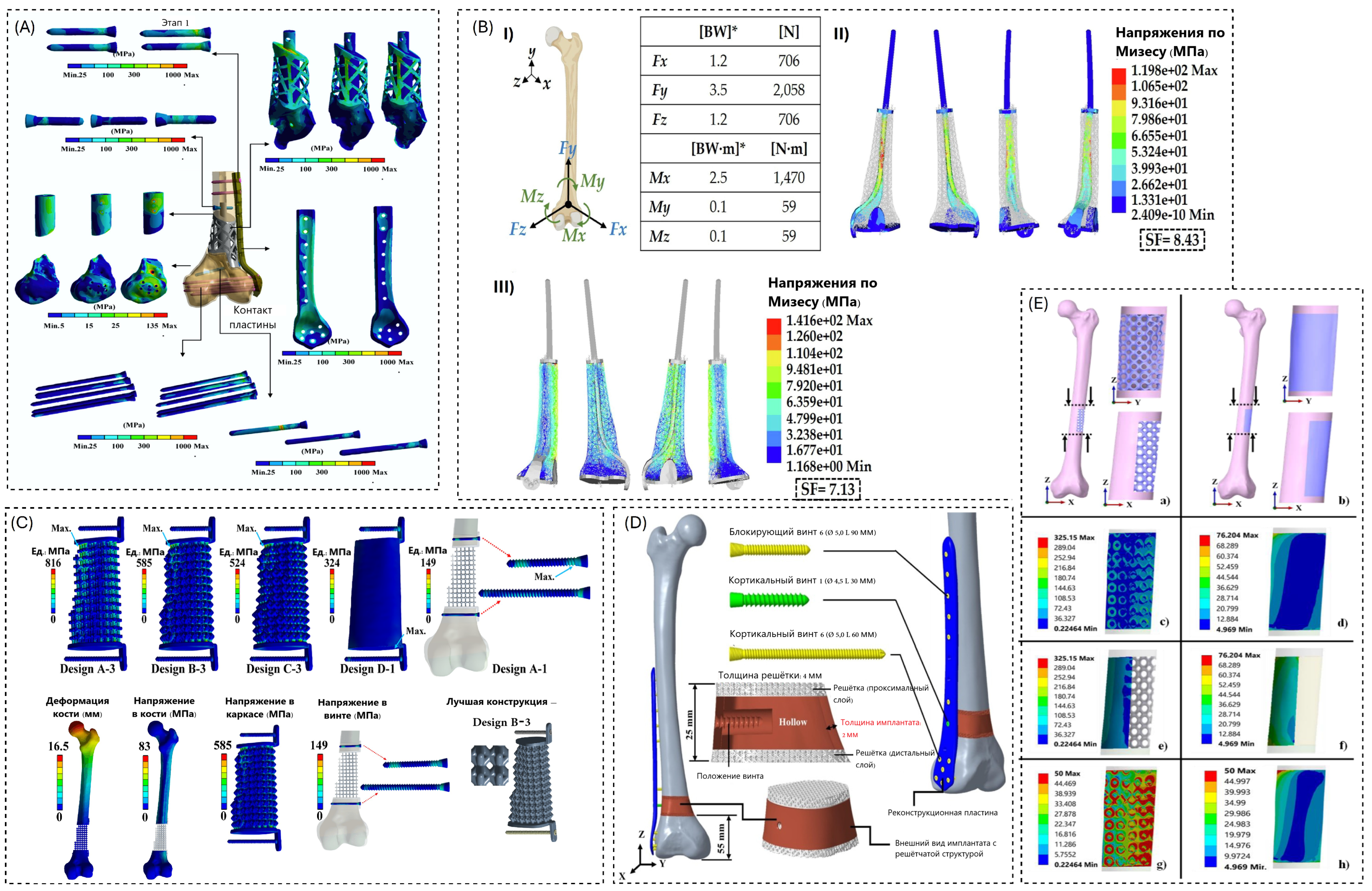
5.2. Экспериментальный обзор: механические испытания, биология и валидация in vivo (E_mech, E_bio, V)

| Год, Ref [n] | Путь | Экспериментальный подход | Испытание/оценка | Выходные данные/метрики | Длительность | Ключевые результаты |
|---|---|---|---|---|---|---|
| 2013, table3.html | E_mech | – Открыто‑пористые образцы Ti6Al4V – SLM или механическая обработка | Одноосное сжатие (уровень образца‑купон) | – Эффективный модуль – Прочность – Кривая «напряжение–деформация» (вход для FE) | Одна серия испытаний | – Получены эффективные свойства для калибровки FE‑модели – Только часть дизайнов обеспечила баланс пористости и стабильности |
| 2014, | E_mech | – Сегментный дефект бедренной кости кадавера – Пустой дефект vs. пористые Ti‑импланты (3 уровня жёсткости) | – Ex vivo осевая компрессия до разрушения – Тензодатчики на пластине и импланте | – Деформация пластины (3 точки) – Деформация импланта – Показатель распределения нагрузки (ε₄) – Групповая статистика | Одно ex vivo‑испытание (n = 20; 5/группа) | – Большая вариабельность в распределении нагрузки – Отсутствие значимых различий по жёсткости между группами – Схема фиксации малочувствительна к небольшим изменениям жёсткости |
| 2019, frontiersin | E_mech | – 3D‑печатные полимерные кубы – Цилиндрический каркас в синтетической бедренной кости + пластина | – Сжатие до 500 N – 3D‑картирование деформаций методом DIC | – Эффективный модуль – Поле перемещений/деформаций по всему объёму – Энергия деформации | Одна серия испытаний | – Гомогенизированная модель воспроизвела глобальную жёсткость и поля деформаций – Практическая неразрушающая характеристизация конструкции в целом |
| 2019, intechopen | E_mech | – Каркасы PLA–β‑TCP/HA – Сферические поры vs. gyroid vs. TO – Несколько уровней пористости | Сжатие до/после деградации | – Модуль – Прочность – Изменение кривой «напряжение–деформация» во времени – Наблюдение микроструктуры | Несколько временных точек (недели) | – Gyroid и TO сохраняли более высокую жёсткость/прочность – Микроструктура снижала потерю прочности, связанную с деградацией |
| 2019, | E_mech | – Каркасы из ABS, полученные FDM – Блочные слои + сегмент бедренной кости на основе КТ – Сотовый заполнитель – 4 растровых шаблона | – Квазистатическое сжатие – До уменьшения высоты на 10% | – Пористость (2 метода) – Прочность (1.76–9.34 MPa) – Модуль (52–212 MPa) – Связи «процесс–свойства» | Одно монотонное испытание | – Достижима высокая пористость (~83%) – Растровый рисунок/воздушный зазор настраивают модуль и прочность |
| 2019, ijmmm.ustb | E_bio + C | – Индуцированные мембраны человека – Вторая стадия по Masquelet – Индивидуальные Ti‑кейджи | – Гистология (окраска по Массону трихромом) – IHC (сосудистые/остеогенные маркеры) – qRT‑PCR vs. фасция | – Морфология мембраны – IHC‑окрашивание – Экспрессия ангиогенных/остеогенных генов | Средний интервал 100 д (83–119 д), n = 5 | – Индуцированные мембраны высоко васкуляризованы – Повышенные ангиогенные/остеогенные сигналы – Подтверждает биологическую роль мембраны вокруг Ti‑кейджей |
| 2020, pmc.ncbi.nlm.nih | E_mech + V | – Биоcерамические импланты TPMS – Дефект бедренной кости крысы (3 mm) – GP vs. GPRC | – Сжатие до разрушения – In vivo + рентген/μCT + гистология | – Прочность/жёсткость при разрушении – Частота переломов – Объём/площадь кости внутри импланта – Пространственное распределение кости | До 8 недель (промежуточно 4–6 нед) | – GP: более высокая пористость, частые переломы – GPRC: улучшенная целостность – Сходный объём кости, но иное распределение |
| 2021, pmc.ncbi.nlm.nih | E_mech | – 3D‑печатные пористые Ti/Ti‑Mg – Регион‑специфические дизайны | Квазистатическое сжатие | – Модуль – Кривая «напряжение–деформация» – Сравнение с FE | Одна серия испытаний | – Экспериментальный модуль близок к FE (~10–15%) – Поддерживает подход согласования жёсткости |
| 2021, scribd | E_mech + V | – Каркас Ti6Al4V ELI с топологией gyroid‑sheet – Критический дефект бедренной кости крысы | – Ex vivo кручение – In vivo μCT + гистология | – Крутильная жёсткость – Момент до разрушения – BV/TV – Гистология интерфейса | 12 недель | – Значительное восстановление крутильной жёсткости – Выраженный рост кости внутрь каркаса – Группа с BMP‑2 показала наибольшее восстановление |
| 2021, sciencedirect | E_mech + V | – Индивидуальный пористый Ti‑имплант – Критический дефект бедренной кости у овцы | – Ex vivo трёхточечный изгиб – In vivo μCT + гистология | – Изгибная жёсткость – Нагрузка разрушения – BV/TV – Сращение на интерфейсе | До 6 месяцев | – Стабильная фиксация – Обширный рост кости внутрь импланта – Отсутствие перелома импланта; жёсткость близка к интактной конечности |
| 2022, rcog | E_mech | – Композитные аналоги бедренной кости – Индивидуальные импланты дистального отдела бедренной кости | – Квазистатическая и циклическая нагрузка – Тензодатчики – Сравнение дизайнов | – Кортікальная деформация – Жёсткость конструкции – Поведение при циклической нагрузке – Согласование с FE | Одна серия испытаний | – Картины деформаций соответствовали FE‑модели – Оптимизированная решётка улучшила физиологические деформации по сравнению со сплошными дизайнами |
| 2023, pmc.ncbi.nlm.nih | E_mech + E_bio | – Ti‑блоки ATS (NP/SP/UP) – С/без кислотного травления (ST) – Одиночные и собранные стопки – Клетки: преостеобласты/hMSCs | – Сжатие (вертикальное/боковое) – Циклическое испытание собранной конструкции (150 N, 0.05 Hz) – μCT/SEM/шероховатость/адсорбция белка – Live/dead, миграция – ARS + RT‑qPCR | – Жёсткость/прочность – Циклическая долговечность – Imbibition – Параметры поверхности – Жизнеспособность/миграция – Остеогенные маркеры (ALP, COL1, RUNX2, OCN) | In vitro до 14 д | – Достаточная прочность и долговечность – ST‑UP показал наилучший биологический ответ – Собранный ATS обеспечил непрерывную миграцию клеток |
| 2023, research.tudelft | E_mech | – CF‑PEEK‑заменитель бедренной кости (FDM) – Геометрия, полученная из КТ | – Сжатие по ISO 7206-4 – Квазистатическое испытание | – Кривая «нагрузка–перемещение» – Общее перемещение – Видимый модуль (apparent stiffness) – Сравнение с FE | Одна серия испытаний | – Результаты испытаний совпали с FE‑моделью – CF‑PEEK подходит в качестве суррогата бедренной кости для испытаний пластин |
| 2023, hal | V | – Биоcерамический каркас из HA – 15 mm метатарзальная кость овцы – Инструментированный кольцевой фиксатор | – In vivo мониторинг усилий – Анализ походки – Оценка жёсткости по КТ‑данным | – GRF – Усилия в фиксаторе/внутренние усилия – Жёсткость мозоли (Kc) – Параметры жёсткости (Kb,p/Kb,d) – TV, CSA, BMD | 70–90 д (8 конечностей) | – Быстрое восстановление распределения нагрузки – Жёсткость возрастала по мере заживления – Механический мониторинг предсказывает траекторию регенерации |
| 2023, riunet.upv | V | – Решётки Ti–19Nb–14Zr – Элементарные ячейки 900/1200 μm – 3 варианта боковых стенок – Больше- и плюсневая кости овцы | – 12 недель in vivo – Ex vivo XCT + ML‑сегментация | – Расстояние BII – Доля BIC – Глубина/объём врастания кости – Сравнение участков | 12 недель | – Конструкции с закрытыми боковыми стенками: сильная интеграция – BII < 10 μm; BIC до ~95% – Меньшие ячейки и закрытие стенок усилили врастание |
| 2024, sciencedirect | E_mech | – Пористые каркасы Ti6Al4V ELI – Радиально‑градиентные дизайны | – Наноиндентирование – Сжатие – До/после снятия остаточных напряжений | – Модуль – Твёрдость – Энергия деформации – Ответ на сжатие | Одна серия испытаний | – Снятие напряжений позволило регулировать жёсткость и энергоёмкость – Низкий модуль при достаточной прочности |
| 2024, pmc.ncbi.nlm.nih | E_mech + E_bio + V | – Импланты дистального бедра Ti: OLS vs. NLS – Биомеханика на 3D‑печатной бедренной кости + пластина – In vitro MG‑63 на дисках – In vivo импланты у свиней (сплошной vs. OLS) | – Биомеханика: 2800 N + тензодатчики – In vitro: MTT‑тест на 24/48/72 h – In vivo: КТ (2/4/8/12 нед) + μCT (9 μm) | – Деформация кости vs. дизайн – FE vs. измеренная деформация (14–17%) – Жизнеспособность клеток (OD) – Плотность/площадь периимплантной кости | – In vitro 72 h – In vivo 12 нед | – OLS обеспечил благоприятный диапазон деформаций – Хорошая совместимость с MG‑63 – Больше периимплантного образования кости по сравнению со сплошным имплантом |
5.3. Обзор трансляционных и клинических исследований (C)
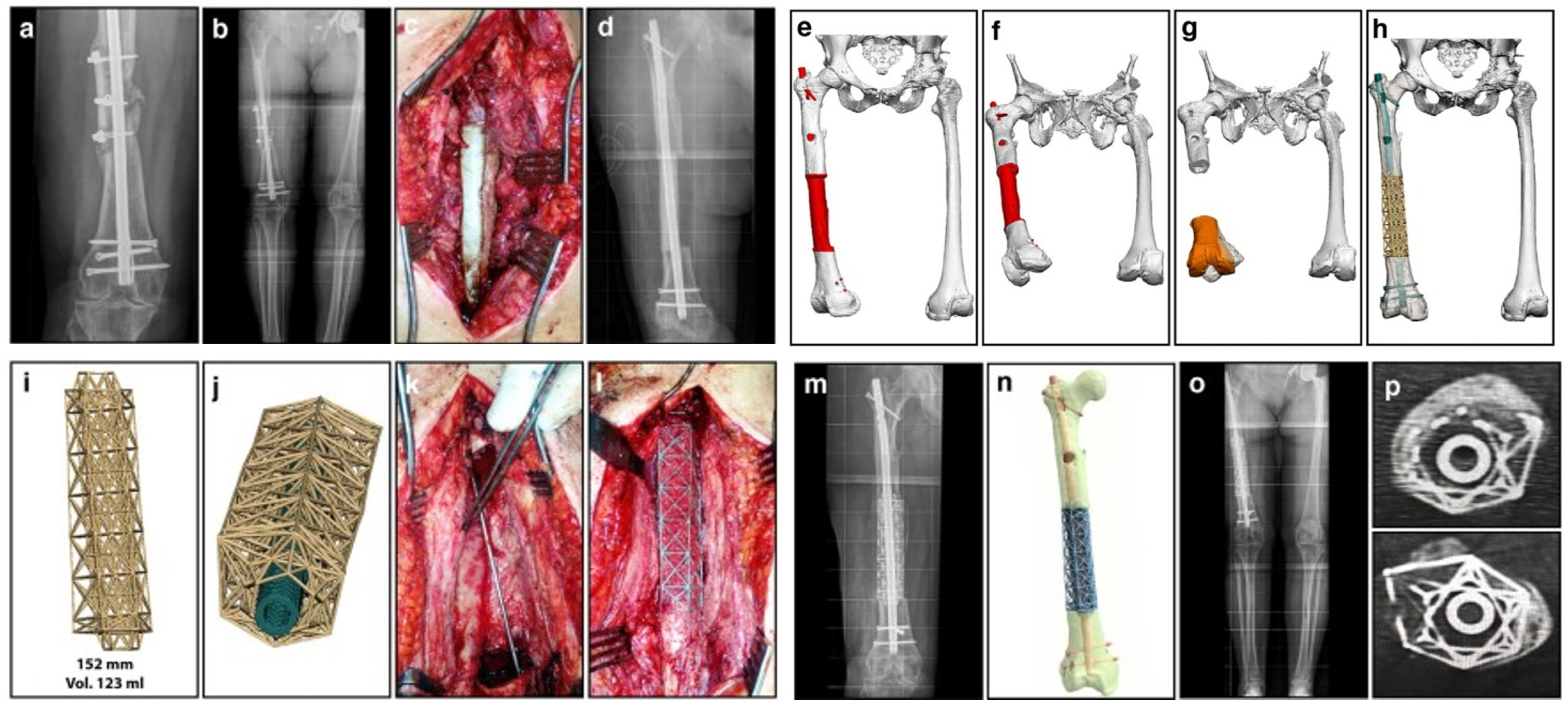
| Год, Ref [n] | Показания и локализация дефекта | Размер/тип дефекта | Имплант/реконструктивная стратегия | N | Наблюдение | Результаты и осложнения (ключевые моменты) |
|---|---|---|---|---|---|---|
| 2019, ijmmm.ustb | Посттравматическая сегментарная потеря бедренной кости; дистальный диафиз/метадиофиз бедренной кости | Сегментарные дефекты критического размера после открытых переломов Grade 3B или дебридмента инфицированных несращений; многосантиметровая потеря кости (до ≈15 cm) | Двухэтапный протокол Masquelet: первоначальный PMMA‑спейсер и индуцированная мембрана, затем индивидуальный 3D‑печатный Ti‑кейдж, заполненный костным трансплантатом и фиксированный интрамедуллярным гвоздём или латеральной блокируемой пластиной | 5 | 12–33 месяцев (среднее 22 месяца) | – Сращение достигнуто во всех случаях – Отсутствие глубокой инфекции или поломки импланта – Хорошее сохранение конечности и функции |
| 2021, sciencedirect | Большие сегментарные дефекты позвоночника, таза и бедренной кости после резекции опухоли или травмы | Многосантиметровые нагружаемые дефекты | Индивидуализированные пористые Ti‑импланты, спроектированные с учётом сращения на интерфейсе «имплант–кость» | 3 | ~12–24 месяца | – Стабильное рентгенологическое сращение – Без расшатывания или перелома – Серьёзные осложнения не отмечены |
6. Критические ограничения и существующие пробелы
6.1. Ограничения КТ и персонализации
6.2. Ограничения моделирования и проверки методом конечных элементов
6.3. Аддитивное производство и отклонения в процессе изготовления
6.4. Ограничения клинического перевода
7. Вызовы и перспективы развития
Клинические рабочие процессы и барьеры на пути внедрения результатов исследований в практику.
8. Выводы и перспективы
Дополнительные материалы
Вклад авторов
Сокращения
| АБС | Акрилонитрилбутадиенстирол |
| АЛЬП | Щелочная фосфатаза |
| ЯВЛЯЮСЬ | Аддитивное производство |
| АО | Рабочая группа по вопросам остеосинтеза |
| АРС | Ализариновый красный S |
| АТС | Сборный титановый каркас |
| до н.э. | Граничные условия |
| БИК | Контакт кости и имплантата |
| БИИ | Расстояние между костью и имплантатом |
| BMD | Плотность костной ткани |
| БМП-2 | Костный морфогенетический белок 2 |
| BSE-SEM | Сканирующая электронная микроскопия в режиме обратнорассеянных электронов |
| БВ/ТВ | Объем костной ткани/общий объем |
| С | Клинические данные (клиническое исследование) |
| САПР | Компьютерное проектирование |
| CAE | Компьютерное проектирование |
| CF-PEEK | Поли(эфир-эфир-кетон), армированный углеродным волокном |
| КОЛ1 | коллаген типа I |
| CPP | Фаза/порошок фосфата кальция |
| КТ | Компьютерная томография |
| ДЕКСА | Двухэнергетическая рентгеновская абсорбциометрия |
| ДИК | Цифровая корреляция изображений |
| DICOM | Цифровая визуализация и связь в медицине |
| ДИВ | Прямое письмо чернилами |
| ДМЛС | Прямое лазерное спекание металла |
| Министерство обороны | Drop-on-Demand |
| DOE | Планирование экспериментов |
| E_bio | биологические эксперименты in vitro |
| E_mech | Механические эксперименты in vitro |
| ЭБМ | Плавление электронным пучком |
| EDM | Электроэрозионная обработка |
| ЭТ | Время контакта |
| ФДМ | Моделирование методом послойного наплавления |
| ФЭ | Конечный элемент |
| МКЭ | Метод/модель конечных элементов |
| ФГМ | Функционально-градиентный материал |
| ФГЛ | Функционально-градиентная решетка |
| FP | Параметр признака |
| ИК-спектроскопия | Фурье-преобразовательная инфракрасная спектроскопия |
| GPRC | G-белковый рецептор |
| ГРФ | Сила реакции опоры |
| HA | Гидроксиапатит |
| HD | Расстояние между люками |
| БЕДРО | Горячее изостатическое прессование |
| ХУ | подразделение Хаунсфилд |
| ИГХ | Иммуногистохимия |
| ИЛ-6 | Интерлейкин-6 |
| Я | Внутрикостный |
| LPBF | Лазерное спекание порошкового слоя |
| ЛТ | Толщина слоя |
| ML | Машинное обучение |
| mPCL–TCP | Полиэтилен медицинского классаϵ-капролактон)–трикальцийфосфат |
| МРТ | Магнитно-резонансная томография |
| Национальные институты здравоохранения США | Национальные институты здравоохранения |
| НЛС | Нерешеточная структура |
| НП | Непористый (блок ATS) |
| OCN | Остеокальцин |
| ОЛС | Оптимальная решетчатая структура |
| ПАКС | Система архивирования и передачи изображений |
| PCA | Анатомический протез с пористым покрытием (коленный протез) |
| ПКЛ | Поли(ϵ-капролактон) |
| ПИК | Поли(эфир-эфир-кетон) |
| НОАК | Полимолочная кислота |
| ПММА | Поли(метилметакрилат) |
| ПолиДжет | Процесс струйной печати фотополимерными материалами (PolyJet) |
| PSLIs | Имплантаты с решетчатой структурой, изготовленные с учетом индивидуальных особенностей пациента. |
| РАНКЛ | Активатор рецептора NF-𝜅B-лиганд |
| РИА | Развертка-Ороситель-Аспиратор |
| ROI | Область интересов |
| РТ | Комнатная температура |
| RT-qPCR | Количественная полимеразная цепная реакция с обратной транскрипцией |
| RUNX2 | Транскрипционный фактор 2, связанный с белком Runt |
| РВЕ | Представительный объемный элемент |
| С | Моделирование (численное/метод конечных элементов) |
| СА/ВР | отношение площади поверхности к объему |
| SGBR | Регенерация костной ткани с использованием каркаса |
| SLA | Стереолитография |
| СЛМ | Селективное лазерное плавление |
| СП | Полупористый (блок ATS) |
| СЕБМ | Селективное плавление электронным пучком |
| TCP | Трикальцийфосфат |
| ТГФ-𝛽1 | Трансформирующий фактор роста бета 1 |
| ТХА | Тотальное эндопротезирование тазобедренного сустава |
| Ti6Al4V | Титановый сплав с 6% Al и 4% V |
| Ti6Al4V ELI | Сверхнизкое содержание примесей в сплаве Ti6Al4V |
| TPMS | Тройно-периодическая минимальная поверхность |
| ТКА | Тотальное эндопротезирование коленного сустава |
| ТВ | Общий объем |
| Контроль качества | Гарантия качества |
| UTM | Универсальная испытательная машина |
| В | эксперименты на животных in vivo |
| VEGFA | Фактор роста эндотелия сосудов А |
| XCT | рентгеновская компьютерная томография |
| Рентгенодифракционный анализ | Рентгеновская дифракция |
| ЯГ | Иттрий-алюминиевый гранат |
| ZTM14N | Титановый сплав Ti–19Nb–14Zr |
| μКТ | Микрокомпьютерная томография |
Список литературы
- Wieding, J.; Souffrant, R.; Mittelmeier, W.; Bader, R. Finite element analysis on the biomechanical stability of open porous titanium scaffolds for large segmental bone defects under physiological load conditions. Med. Eng. Phys. 2013, 35, 422–432. [Google Scholar] [CrossRef]
- Tetsworth, K.; Woloszyk, A.; Glatt, V. 3D printed titanium cages combined with the Masquelet technique for the reconstruction of segmental femoral defects: Preliminary clinical results and molecular analysis of the biological activity of human-induced membranes. OTA Int. 2019, 2, e016. [Google Scholar] [CrossRef] [PubMed]
- Wong, K.W.; Wu, C.D.; Chien, C.S.; Lee, C.W.; Yang, T.H.; Lin, C.L. Patient-specific 3-dimensional printing titanium implant biomechanical evaluation for complex distal femoral open fracture reconstruction with segmental large bone defect: A nonlinear finite element analysis. Appl. Sci. 2020, 10, 4098. [Google Scholar] [CrossRef]
- Zhang, T.; Wei, Q.; Zhou, H.; Jing, Z.; Liu, X.; Zheng, Y.; Cai, H.; Wei, F.; Jiang, L.; Yu, M.; et al. Three-dimensional-printed individualized porous implants: A new “implant-bone” interface fusion concept for large bone defect treatment. Bioact. Mater. 2021, 6, 3659–3670. [Google Scholar] [CrossRef]
- Jin, H.; Zhuo, Y.; Sun, Y.; Fu, H.; Han, Z. Microstructure design and degradation performance in vitro of three-dimensional printed bioscaffold for bone tissue engineering. Adv. Mech. Eng. 2019, 11, 1687814019883784. [Google Scholar] [CrossRef]
- Kelly, C.N.; Lin, A.S.; Leguineche, K.E.; Shekhar, S.; Walsh, W.R.; Guldberg, R.E.; Gall, K. Functional repair of critically sized femoral defects treated with bioinspired titanium gyroid-sheet scaffolds. J. Mech. Behav. Biomed. Mater. 2021, 116, 104380. [Google Scholar] [CrossRef]
- Verma, R.; Kumar, J.; Singh, N.K.; Rai, S.K.; Saxena, K.K.; Xu, J. Design and analysis of biomedical scaffolds using TPMS-based porous structures inspired from additive manufacturing. Coatings 2022, 12, 839. [Google Scholar] [CrossRef]
- Lee, S.S.; Du, X.; Smit, T.; Bissacco, E.G.; Seiler, D.; de Wild, M.; Ferguson, S.J. 3D-printed LEGO®-inspired titanium scaffolds for patient-specific regenerative medicine. Biomater. Adv. 2023, 154, 213617. [Google Scholar] [CrossRef]
- Charbonnier, B.; Manassero, M.; Bourguignon, M.; Decambron, A.; El-Hafci, H.; Morin, C.; Leon, D.; Bensidoum, M.; Corsia, S.; Petite, H.; et al. Custom-made macroporous bioceramic implants based on triply-periodic minimal surfaces for bone defects in load-bearing sites. Acta Biomater. 2020, 109, 254–266. [Google Scholar] [CrossRef] [PubMed]
- Blázquez-Carmona, P.; Mora-Macías, J.; Martínez-Vázquez, F.J.; Morgaz, J.; Domínguez, J.; Reina-Romo, E. Mechanics predicts effective critical-size bone regeneration using 3d-printed bioceramic scaffolds. Tissue Eng. Regen. Med. 2023, 20, 893–904. [Google Scholar] [CrossRef]
- Wu, P.K.; Lee, C.W.; Sun, W.H.; Lin, C.L. Biomechanical analysis and design method for patient-specific reconstructive implants for large bone defects of the distal lateral femur. Biosensors 2021, 12, 4. [Google Scholar] [CrossRef]
- Chang, C.M.; Wong, P.C.; Ou, S.L.; Ko, C.E.; Wang, Y.T. Optimizing implant lattice design for large distal femur defects: Stimulating interface bone growth to enhance osseointegration. Int. J. Bioprint. 2024, 10, 2590. [Google Scholar] [CrossRef]
- Obaton, A.F.; Fain, J.; Meinel, D.; Tsamos, A.; Léonard, F.; Lécuelle, B.; Djemaï, M. In vivo bone progression in and around lattice implants additively manufactured with a new titanium alloy. Appl. Sci. 2023, 13, 7282. [Google Scholar] [CrossRef]
- Rana, M.; Chaudhuri, A.; Biswas, J.K.; Karim, S.I.; Datta, P.; Karmakar, S.K.; Roychowdhury, A. Design of patient specific bone stiffness mimicking scaffold. Proc. Inst. Mech. Eng. Part H J. Eng. Med. 2021, 235, 1453–1462. [Google Scholar] [CrossRef] [PubMed]
- Entezari, A.; Zhang, Z.; Sue, A.; Sun, G.; Huo, X.; Chang, C.C.; Zhou, S.; Swain, M.V.; Li, Q. Nondestructive characterization of bone tissue scaffolds for clinical scenarios. J. Mech. Behav. Biomed. Mater. 2019, 89, 150–161. [Google Scholar] [CrossRef]
- Lee, M.C.; Pan, C.T.; Chen, W.F.; Lin, M.C.; Shiue, Y.L. Design, manufacture, and characterization of a critical-sized gradient porosity dual-material tibial defect scaffold. Bioengineering 2024, 11, 308. [Google Scholar] [CrossRef] [PubMed]
- Vasanthanathan, A.; Kennedy, S.M. Bio-printing of femur model: A bone substitute for biomedical research. Mater. Technol. 2023, 57, 283–289. [Google Scholar] [CrossRef]
- Rezapourian, M.; Sadat Mirhakimi, A.; Nematollahi, M.; Minasyan, T.; Hussainova, I. Patient-Specific Lattice Implants for Segmental Femoral and Tibial Reconstruction (Part 1): Defect Patterns, Fixation Strategies and Reconstruction Options—A Review. Biomimetics 2026, 2, 2313–7673. [Google Scholar] [CrossRef]
- Uhthoff, H.K.; Poitras, P.; Backman, D.S. Internal plate fixation of fractures: Short history and recent developments. J. Orthop. Sci. 2006, 11, 118–126. [Google Scholar] [CrossRef] [PubMed]
- Hernigou, P.; Pariat, J. History of internal fixation (part 1): Early developments with wires and plates before World War II. Int. Orthop. 2017, 41, 1273–1283. [Google Scholar] [CrossRef]
- Matter, P. History of the AO and its global effect on operative fracture treatment. Clin. Orthop. Relat. Res. 1998, 347, 11–18. [Google Scholar] [CrossRef]
- Vécsei, V.; Hajdu, S.; Negrin, L.L. Intramedullary nailing in fracture treatment: History, science and Küntscher’s revolutionary influence in Vienna, Austria. Injury 2011, 42, S1–S5. [Google Scholar] [CrossRef]
- Buhl, C. 80 years of intramedullary nailing: New facts and information about a milestone in osteosynthesis. Der Unfallchirurg 2019, 122, 127–133. [Google Scholar] [CrossRef]
- Aktuglu, K.; Erol, K.; Vahabi, A. Ilizarov bone transport and treatment of critical-sized tibial bone defects: A narrative review. J. Orthop. Traumatol. 2019, 20, 22. [Google Scholar] [CrossRef]
- Chaddha, M.; Gulati, D.; Singh, A.P.; Singh, A.P.; Maini, L. Management of massive posttraumatic bone defects in the lower limb with the Ilizarov technique. Acta Orthop. Belg. 2010, 76, 811. [Google Scholar]
- Schulz, R.A.; Stein, J.A.; Pelc, N.J. How CT happened: The early development of medical computed tomography. J. Med. Imaging 2021, 8, 052110. [Google Scholar] [CrossRef]
- GNHounsfield.org. Firsts. 2021. Available online: https://gnhounsfield.org/Firsts.html (accessed on 3 November 2025).
- Alford, A.I.; Nicolaou, D.; Hake, M.; McBride-Gagyi, S. Masquelet’s induced membrane technique: Review of current concepts and future directions. J. Orthop. Res. 2021, 39, 707–718. [Google Scholar] [CrossRef]
- Masquelet, A.C. The induced membrane technique. Orthop. Traumatol. Surg. Res. 2020, 106, 785–787. [Google Scholar] [CrossRef] [PubMed]
- Han, W.; Shen, J.; Wu, H.; Yu, S.; Fu, J.; Xie, Z. Induced membrane technique: Advances in the management of bone defects. Int. J. Surg. 2017, 42, 110–116. [Google Scholar] [CrossRef] [PubMed]
- Kubiak, E.N.; Fulkerson, E.; Strauss, E.; Egol, K.A. The evolution of locked plates. J. Bone Jt. Surg. 2006, 88, 189–200. [Google Scholar]
- Cronier, P.; Pietu, G.; Dujardin, C.; Bigorre, N.; Ducellier, F.; Gerard, R. The concept of locking plates. Orthop. Traumatol. Surg. Res. 2010, 96, S17–S36. [Google Scholar] [CrossRef]
- Haidukewych, G.J. Innovations in locking plate technology. JAAOS-J. Am. Acad. Orthop. Surg. 2004, 12, 205–212. [Google Scholar] [CrossRef]
- Garabano, G.; Del Sel, H.; Rodriguez, J.A.; Perez Alamino, L.; Pesciallo, C.A. The effectiveness of antibiotic cement-coated nails in post-traumatic femoral and tibial osteomyelitis–comparative analysis of custom-made versus commercially available nails. J. Bone Jt. Infect. 2021, 6, 457–466. [Google Scholar] [CrossRef]
- Ghaseminejad-Raeini, A.; Azarboo, A.; Pirahesh, K.; Sharafi, A.; Hoveidaei, A.H.; Nwankwo, B.O.; Annasamudram, A.; Conway, J.D. Antibiotic-coated intramedullary nailing managing long bone infected non-unions: A meta-analysis of comparative studies. Antibiotics 2024, 13, 69. [Google Scholar] [CrossRef] [PubMed]
- Summers, S.; Krkovic, M. Bone transport with magnetic intramedullary nails in long bone defects. Eur. J. Orthop. Surg. Traumatol. 2021, 31, 1243–1252. [Google Scholar] [CrossRef] [PubMed]
- Smolle, M.A.; Zötsch, S.; Andreou, D.; Valentini, M.; Leithner, A.; Lanz, P. Bone transport nails for reconstruction of lower limb diaphyseal defects in patients with bone sarcomas: A case series. Wien. Klin. Wochenschr. 2025, 137, 654–660. [Google Scholar] [CrossRef]
- Cobos, J.A.; Lindsey, R.W.; Gugala, Z. The cylindrical titanium mesh cage for treatment of a long bone segmental defect: Description of a new technique and report of two cases. J. Orthop. Trauma 2000, 14, 54–59. [Google Scholar] [CrossRef]
- Dvorak, M.F.; Kwon, B.K.; Fisher, C.G.; Eiserloh, H.L., III; Boyd, M.; Wing, P.C. Effectiveness of titanium mesh cylindrical cages in anterior column reconstruction after thoracic and lumbar vertebral body resection. Spine 2003, 28, 902–908. [Google Scholar] [CrossRef]
- Toosi, S.; Javid-Naderi, M.J.; Tamayol, A.; Ebrahimzadeh, M.H.; Yaghoubian, S.; Mousavi Shaegh, S.A. Additively manufactured porous scaffolds by design for treatment of bone defects. Front. Bioeng. Biotechnol. 2024, 11, 1252636. [Google Scholar] [CrossRef]
- Deering, J.; Dowling, K.I.; DiCecco, L.A.; McLean, G.D.; Yu, B.; Grandfield, K. Selective Voronoi tessellation as a method to design anisotropic and biomimetic implants. J. Mech. Behav. Biomed. Mater. 2021, 116, 104361. [Google Scholar] [CrossRef] [PubMed]
- sadat Mirhakimi, A.; Dubey, D.; Elbestawi, M.A. Laser powder bed fusion of bio-inspired metamaterials for energy absorption applications: A review. J. Mater. Res. Technol. 2024, 31, 2126–2155. [Google Scholar] [CrossRef]
- Müller, P.; Synek, A.; Stauß, T.; Steinnagel, C.; Ehlers, T.; Gembarski, P.C.; Pahr, D.; Lachmayer, R. Development of a density-based topology optimization of homogenized lattice structures for individualized hip endoprostheses and validation using micro-FE. Sci. Rep. 2024, 14, 5719. [Google Scholar] [CrossRef] [PubMed]
- Davoodi, E.; Montazerian, H.; Mirhakimi, A.S.; Zhianmanesh, M.; Ibhadode, O.; Shahabad, S.I.; Esmaeilizadeh, R.; Sarikhani, E.; Toorandaz, S.; Sarabi, S.A.; et al. Additively manufactured metallic biomaterials. Bioact. Mater. 2022, 15, 214–249. [Google Scholar] [CrossRef]
- Kadkhodapour, J.; Mirhakimi, A.S.; Montazerian, H. Structural defects and mechanical properties of additively manufactured parts. In Quality Analysis of Additively Manufactured Metals; Elsevier: Amsterdam, The Netherlands, 2023; pp. 119–172. [Google Scholar]
- Schick, V.D.; Zampogna, B.; Marrara, G.; Siracusano, L.; Larizza, L.; Calaciura, S.; Sanzarello, I.; Marinozzi, A.; Leonetti, D. Custom-Made 3D-Printed Titanium Implants for Managing Segmental Distal Tibial Bone Defects: A Systematic Literature Review. J. Clin. Med. 2025, 14, 1796. [Google Scholar] [CrossRef]
- Castrisos, G.; Matheus, I.G.; Sparks, D.; Lowe, M.; Ward, N.; Sehu, M.; Wille, M.L.; Phua, Y.; Savi, F.M.; Hutmacher, D.; et al. Regenerative matching axial vascularisation of absorbable 3D-printed scaffold for large bone defects: A first in human series. J. Plast. Reconstr. Aesthetic Surg. 2022, 75, 2108–2118. [Google Scholar] [CrossRef]
- Sparks, D.S.; Savi, F.M.; Dlaska, C.E.; Saifzadeh, S.; Brierly, G.; Ren, E.; Cipitria, A.; Reichert, J.C.; Wille, M.L.; Schuetz, M.A.; et al. Convergence of scaffold-guided bone regeneration principles and microvascular tissue transfer surgery. Sci. Adv. 2023, 9, eadd6071. [Google Scholar] [CrossRef]
- Sparks, D.S.; Wiper, J.; Lloyd, T.; Wille, M.L.; Sehu, M.; Savi, F.M.; Ward, N.; Hutmacher, D.W.; Wagels, M. Protocol for the BONE-RECON trial: A single-arm feasibility trial for critical sized lower limb BONE defect RECONstruction using the mPCL-TCP scaffold system with autologous vascularised corticoperiosteal tissue transfer. BMJ Open 2023, 13, e056440. [Google Scholar] [CrossRef]
- McAnena, A.P.; McClennen, T.; Zheng, H. Patient-specific 3-dimensional-printed orthopedic implants and surgical devices are potential alternatives to conventional technology but require additional characterization. Clin. Orthop. Surg. 2024, 17, 1. [Google Scholar] [CrossRef]
- Yon, C.J.; Choi, B.C.; Lee, J.M.; Lee, S.W. Personalized 3D-Printed Prostheses for Bone Defect Reconstruction After Tumor Resection in the Foot and Ankle. J. Funct. Biomater. 2025, 16, 62. [Google Scholar] [CrossRef]
- Campanacci, L.; Cevolani, L.; Focaccia, M.; Di Gennaro, G.L.; Dozza, B.; Staals, E.; Zuccheri, F.; Bianchi, G.; Donati, D.M.; Manfrini, M. Lengthening patients previously treated for massive lower limb reconstruction for bone tumors with the PRECICE 2 Nail. Children 2023, 10, 1772. [Google Scholar] [CrossRef] [PubMed]
- Rosslenbroich, S.B.; Oh, C.W.; Kern, T.; Mukhopadhaya, J.; Raschke, M.J.; Kneser, U.; Krettek, C. Current management of diaphyseal long bone defects—a multidisciplinary and international perspective. J. Clin. Med. 2023, 12, 6283. [Google Scholar] [CrossRef]
- Solanki, T.; Maurya, M.K.; Singh, P.K. Results of antibiotic-impregnated cement/polymer-coated intramedullary nails in the management of infected nonunion and open fractures of long bones. Cureus 2023, 15. [Google Scholar] [CrossRef]
- Anaspure, O.S.; Patel, S.; Baumann, A.N.; Anastasio, A.T.; Pean, C.; DeBaun, M.R. Nail–Plate Constructs for Treating Distal Femur Fractures: A Systematic Review of Biomechanical Studies. Surgeries 2024, 5, 799–816. [Google Scholar] [CrossRef]
- Alkentar, R.; Máté, F.; Mankovits, T. Investigation of the performance of Ti6Al4V lattice structures designed for biomedical implants using the finite element method. Materials 2022, 15, 6335. [Google Scholar] [CrossRef] [PubMed]
- Di Caprio, F.; Franchitti, S.; Borrelli, R.; Bellini, C.; Di Cocco, V.; Sorrentino, L. Ti-6Al-4V octet-truss lattice structures under bending load conditions: Numerical and experimental results. Metals 2022, 12, 410. [Google Scholar] [CrossRef]
- Crovace, A.M.; Lacitignola, L.; Forleo, D.M.; Staffieri, F.; Francioso, E.; Di Meo, A.; Becerra, J.; Crovace, A.; Santos-Ruiz, L. 3D biomimetic porous titanium (Ti6Al4V ELI) scaffolds for large bone critical defect reconstruction: An experimental study in sheep. Animals 2020, 10, 1389. [Google Scholar] [CrossRef]
- Laubach, M.; Suresh, S.; Herath, B.; Wille, M.L.; Delbrück, H.; Alabdulrahman, H.; Hutmacher, D.W.; Hildebrand, F. Clinical translation of a patient-specific scaffold-guided bone regeneration concept in four cases with large long bone defects. J. Orthop. Transl. 2022, 34, 73–84. [Google Scholar] [CrossRef] [PubMed]
- Kang, K.W.; Yang, S.; Kim, S.Y.; Choi, J.; Kang, B.J. Integration of locking screw fixation into 3D-printed patient-specific porous titanium implants enhances osseointegration: An in vivo study in a rabbit bone defect model. J. Vet. Sci. 2025, 26, e62. [Google Scholar] [CrossRef] [PubMed]
- Christodoulou, M.; Hadjipolydorou, N.; Christofi, E.; Orfanos, I. Bone transport using an intramedullary magnetic nail in a femur with chronic osteomyelitis after a car bomb attack in Somalia: A case report. J. Orthop. Rep. 2025, 4, 100376. [Google Scholar] [CrossRef]
- Liu, L.; Liu, C.; Deng, C.; Wang, X.; Liu, X.; Luo, M.; Wang, S.; Liu, J. Design and performance analysis of 3D-printed stiffness gradient femoral scaffold. J. Orthop. Surg. Res. 2023, 18, 120. [Google Scholar] [CrossRef]
- Lu, H.T.; Hsu, C.C.; Jian, Q.Q.; Chen, W.T. Biomechanical Study of Different Scaffold Designs for Reconstructing a Traumatic Distal Femur Defect Using Patient-Specific Computational Modeling. Comput. Model. Eng. Sci. 2025, 142, 1883–1898. [Google Scholar] [CrossRef]
- Shams, M.; Mansurov, Z.; Daulbayev, C.; Bakbolat, B. Effect of Lattice Structure and Composite Precursor on Mechanical Properties of 3D-Printed Bone Scaffolds. Eurasian Chem.-Technol. J. 2021, 23, 257–266. [Google Scholar] [CrossRef]
- Bayoglu, R.; Okyar, A.F. Implementation of boundary conditions in modeling the femur is critical for the evaluation of distal intramedullary nailing. Med. Eng. Phys. 2015, 37, 1053–1060. [Google Scholar] [CrossRef]
- Acar, A.A.; Daskalakis, E.; Bartolo, P.; Weightman, A.; Cooper, G.; Blunn, G.; Koc, B. Customized scaffolds for large bone defects using 3D-printed modular blocks from 2D-medical images. Bio-Des. Manuf. 2024, 7, 74–87. [Google Scholar] [CrossRef]
- Karuppudaiyan, S.; Singh, D.K.J.; Santosh, V.M. Finite element analysis of scaffold for large defect in femur bone. In Proceedings of the IOP Conference Series: Materials Science and Engineering; IOP Publishing: Bristol, UK, 2018; Volume 402, p. 012096. [Google Scholar]
- Pobloth, A.M.; Checa, S.; Razi, H.; Petersen, A.; Weaver, J.C.; Schmidt-Bleek, K.; Windolf, M.; Tatai, A.Á.; Roth, C.P.; Schaser, K.D.; et al. Mechanobiologically optimized 3D titanium-mesh scaffolds enhance bone regeneration in critical segmental defects in sheep. Sci. Transl. Med. 2018, 10, eaam8828. [Google Scholar] [CrossRef] [PubMed]
- Karuppudaiyan, S.; Singh, D.K.J. Design of scaffold with controlled internal architecture using fused deposition modeling (FDM). Int. J. Eng. Adv. Technol. 2019, 9, 2764–2768. [Google Scholar] [CrossRef]
- Yavari, S.A.; van der Stok, J.; Ahmadi, S.; Wauthlé, R.; Schrooten, J.; Weinans, H.; Zadpoor, A.A. Mechanical analysis of a rodent segmental bone defect model: The effects of internal fixation and implant stiffness on load transfer. J. Biomech. 2014, 47, 2700–2708. [Google Scholar] [CrossRef]
- Lindsey, R.W.; Gugala, Z.; Milne, E.; Sun, M.; Gannon, F.H.; Latta, L.L. The efficacy of cylindrical titanium mesh cage for the reconstruction of a critical-size canine segmental femoral diaphyseal defect. J. Orthop. Res. 2006, 24, 1438–1453. [Google Scholar] [CrossRef]
- Park, J.W.; Kang, H.G.; Kim, J.H.; Kim, H.S. New 3-dimensional implant application as an alternative to allograft in limb salvage surgery: A technical note on 10 cases. Acta Orthop. 2020, 91, 489–496. [Google Scholar] [CrossRef]
- Guder, W.K.; Hardes, J.; Nottrott, M.; Podleska, L.E.; Streitbürger, A. Highly cancellous titanium alloy (TiAl6V4) surfaces on three-dimensionally printed, custom-made intercalary tibia prostheses: Promising short-to intermediate-term results. J. Pers. Med. 2021, 11, 351. [Google Scholar] [CrossRef]
- Li, J.; Wang, L.; He, X.; Liang, J.; Dong, C. Additively manufactured metallic TPMS lattice structures: Design strategies, fabrication, multifunctional properties, and applications. NPJ Adv. Manuf. 2025, 2, 45. [Google Scholar] [CrossRef]
- Wei, J.; Gross, D.; Lane, N.E.; Lu, N.; Wang, M.; Zeng, C.; Yang, T.; Lei, G.; Choi, H.K.; Zhang, Y. Risk factor heterogeneity for medial and lateral compartment knee osteoarthritis: Analysis of two prospective cohorts. Osteoarthr. Cartil. 2019, 27, 603–610. [Google Scholar] [CrossRef]
- Li, L.; Shi, J.; Zhang, K.; Yang, L.; Yu, F.; Zhu, L.; Liang, H.; Wang, X.; Jiang, Q. Early osteointegration evaluation of porous Ti6Al4V scaffolds designed based on triply periodic minimal surface models. J. Orthop. Transl. 2019, 19, 94–105. [Google Scholar] [CrossRef]
- Benady, A.; Meyer, S.J.; Golden, E.; Dadia, S.; Levy, G.K. Patient-specific Ti-6Al-4V lattice implants for critical-sized load-bearing bone defects reconstruction. Mater. Des. 2023, 226, 111605. [Google Scholar] [CrossRef]
- Wong, K.W.; Wu, C.D.; Chien, C.S.; Lee, C.W.; Yang, T.H. Patient-Specific 3D-Printed Titanium Implant for Complex Distal Femoral Open Fracture Reconstruction with Segmental Large Defect. Appl. Sci. 2020, 10, 4098. [Google Scholar] [CrossRef]
- Tetsworth, K.; Block, S.; Glatt, V. Putting 3D modelling and 3D printing into practice: Virtual surgery and preoperative planning to reconstruct complex post-traumatic skeletal deformities and defects. Sicot-J 2017, 3, 16. [Google Scholar] [CrossRef] [PubMed]