Источник: Biomimetics 2026, 11(2), 128
DOI: https://doi.org/10.3390/biomimetics11020128
Авторы: Mansoureh Rezapourian, Anooshe Sadat Mirhakimi, Mahan Nematollahi, Tatevik Minasyan, Irina Hussainova
Перевод с английского
Аннотация
В данной первой части двухчастного обзора рассматривается применение пористых имплантатов, изготовленных методами аддитивного производства (АП) на основе данных компьютерной томографии (CT), для замещения крупных сегментарных дефектов бедренной и большеберцовой костей. Рассматриваются лёгкие пациент-специфичные имплантаты с решётчатой структурой, каркасы с заданной архитектурой и модульные пористые конструкции, в которых инженерная пористость интегрирована в несущую структуру и применяется совместно со стабилизацией на основе пластин, гвоздей или аппаратов внешней фиксации. Показано, как дефекты описываются и классифицируются по размеру, морфологии и анатомическому субсегменту; как эти характеристики влияют на выбор способа фиксации и возникающую механическую среду; и в каких отделах бедренной и большеберцовой костей пористые имплантаты применялись в клинических и доклинических условиях. По данным литературы, исходы лечения в наибольшей мере определяются морфологией дефекта и состоянием местной биологической среды, тогда как осуществимость фиксации и поведение конструкции варьируют в зависимости от субрегиональной анатомии. В большинстве описанных конструкций используются Ti6Al4V пористые архитектуры, предназначенные для совместного восприятия нагрузки с фиксирующей системой, снижения экранирования напряжений и создания регенеративного пространства для приживления трансплантата и врастания тканей. Результаты метода конечных элементов (FEA) и стендовых испытаний неизменно показывают, что архитектура решётчатой структуры, относительная плотность (RD) и концепция фиксации совместно определяют жёсткость, микроподвижность и зоны, критичные с точки зрения усталостного разрушения, тогда как ранние данные на животных и у людей свидетельствуют об обнадёживающей интеграции имплантата и восстановлении функции в отдельных случаях крупных дефектов. Вместе с тем дескрипторы дефектов, описание фиксации, граничные условия и метрики исходов остаются разнообразными, а явная количественная валидация результатов моделирования с механическими или прижизненными измерениями встречается редко. Большинство опубликованных работ опирается на моделирование и стендовые испытания при ограниченном отражении биологических конечных точек, что образует «валидационный разрыв», препятствующий прямой клинической трансляции. Подчёркивается необходимость стандартизированных дескрипторов дефектов и фиксации, согласованных механических и расчётных протоколов, а также дефект-ориентированных наборов данных, интегрирующих анатомические, механические, биологические и клинические данные, — без чего практический перевод результатов в клинику невозможен.
Ключевые слова: пациент-специфичные имплантаты; сегментарные дефекты длинных трубчатых костей; CT-планирование хирургических вмешательств; пористые костные скаффолды; стратегии фиксации; механобиология; сегментарные дефекты бедренной и большеберцовой костей; критически большие дефекты костей; 3D-печатные пористые скаффолды; имплантаты с решётчатой структурой; аддитивное производство в ортопедии; скаффолд-направляемая регенерация кости; фиксация блокирующей пластиной; экранирование напряжений; реконструкция бедренной и большеберцовой костей; несущая функция; персонализированная тканевая инженерия кости
1. Введение
Сегментарные диафизарные дефекты бедренной и большеберцовой костей относятся к наиболее сложным задачам восстановительной хирургии конечностей. Даже при использовании современных методов — дистракционного остеогенеза и двухэтапной методики индуцированной мембраны Masquelet — эти дефекты трудно поддаются лечению. При применении васкуляризированных костных трансплантатов и мегапротезов необходимо учитывать, что достижение сращения нередко требует длительного периода лечения, который является непременным условием оптимального восстановления. Недавние обзоры, посвящённые посттравматическим дефектам большеберцовой кости и реконструкциям с применением методики индуцированной мембраны, сообщают о частоте осложнений, включающих инфекции, нарушения оси конечности и потребность в повторных вмешательствах, несмотря на высокий общий уровень сращения, что свидетельствует о биологической и механической нестабильности подобных реконструкций [1,2,3]. Сохраняющиеся трудности стимулируют всё больший интерес к методам, способным эффективно сочетать немедленную механическую стабильность с благоприятной для кости средой в крупных дефектах бедренной и большеберцовой костей.
Аддитивное производство (АП) претерпело трансформацию от экспериментального применения к рутинному использованию для создания пациент-специфичных имплантатов (PSI) в онкологической хирургии и при сложных травмах. Серии наблюдений и систематические обзоры, посвящённые индивидуальным 3D-печатным устройствам при диафизарных и дистальных дефектах большеберцовой кости, показывают, что PSI способны эффективно восстанавливать длину и ось конечности, упрощать реконструкцию нестандартных дефектов и снижать потребность в массивных аллотрансплантатах. Вместе с тем необходимо учитывать, что сроки наблюдения в этих исследованиях остаются относительно короткими, а профили осложнений существенно варьируют [4,5].
В последнее время персонализированные имплантаты с решётчатой или ферменной структурой, включающие интегрированные отверстия для винтов и ножки, стали появляться как альтернатива традиционным кейджам и мегапротезам, демонстрируя в отдельных случаях крупных дефектов раннюю остеоинтеграцию и улучшение функции [6]. Эти достижения наглядно демонстрируют эффективность конструкций, спланированных на основе CT и изготовленных методами АП, которые объединяют в едином устройстве фиксацию, заполнение дефекта и сустав-сохраняющую реконструкцию.
Параллельно архитектурированные пористые материалы превратились в обширное пространство для разработки костных заменителей. Недавние исследования показывают, что решётчатые структуры, имитирующие кость, могут быть настроены на соответствие кости по жёсткости, прочности, долговечности при усталостном нагружении и проницаемости путём изменения типа элементарной ячейки, относительной плотности (RD) и архитектурных градиентов — без изменения свойств основного сплава [7,8,9,10]. Такие решётчатые структуры обеспечивают взаимосвязанную пористость для сосудистого и костного врастания, допуская при этом управляемую передачу нагрузки на кость-хозяина. Данный подход непосредственно решает давние проблемы экранирования напряжений и асептического расшатывания при плотных интеркалярных трансплантатах и мегапротезах [11].
Совершенствование клинической практики и материалов в значительной мере опирается на планирование на основе изображений и численное моделирование. Пациент-специфичные конечно-элементные (FE) рабочие процессы в настоящее время позволяют интегрировать CT-геометрию бедренной и большеберцовой костей с конкретными условиями нагружения для дооперационной оценки жёсткости имплантата, траекторий винтов и распределения деформаций в кости [12,13]. Ряд недавних исследований расширил эту концепцию применительно к имплантатам АП с решётчатой структурой: для разработки рекомендаций по проектированию дистальных реконструкций бедренной кости или валидации пациент-специфичных решётчатых сегментов при дефектах бедренной кости использовались FE-анализ и топологическая оптимизация с верификацией на экспериментальных данных [14,15]. Тем не менее имеющиеся данные остаются неполными и разнородными. Различные группы исследователей сосредоточиваются на классификации дефектов, стратегиях фиксации, архитектуре решётчатых структур или методологии моделирования, и лишь немногие объединяют все эти элементы в единый рабочий процесс «от дефекта к конструкции» [16].
Данная первая часть нашего двухчастного обзора посвящена сегментарным дефектам бедренной и большеберцовой костей, реконструируемым с помощью изготовленных методами АП пористых имплантатов на основе CT. Рассматриваются реконструкции, в которых инженерная пористость интегрирована в несущую структуру. Это включает пациент-специфичные имплантаты с решётчатой структурой, модульные пористые блоки и каркасы с заданной архитектурой, применяемые в сочетании с пластинами, гвоздями или аппаратами внешней фиксации. Стандартные костные заменители и плотные, непористые мегапротезы не являются предметом данного двухчастного обзора. Часть I преследует три цели: 1) описать, как в клинических сериях и доклинических моделях характеризуются типы дефектов и как эти характеристики влияют на стратегии фиксации и механическую среду; 2) создать обзор анатомических и фиксационных данных по задокументированным реконструкциям бедренной и большеберцовой костей с акцентом на применение пористых имплантатов при различных сегментах и размерах дефектов; 3) объединить механические данные из моделирования и экспериментов, подтверждающие данные концепции. Таким образом создаётся механобиологическая основа для проектирования и интерпретации PSLI (пациент-специфичных имплантатов с решётчатой структурой), применяемых при сегментарной реконструкции бедренной и большеберцовой костей; сопутствующий обзор Части 2 посвящён рабочим процессам CT → имплантат, стратегиям проектирования решётчатых структур, маршрутам аддитивного производства и детальному методологическому описанию экспериментальной, расчётной, биологической и клинической валидации.
Обзор выполнен в форме структурированного нарратива. Проводился целенаправленный поиск в базах данных PubMed/MEDLINE и Google Scholar (а также Scopus/Web of Science при их доступности) за период с 2013 по 2025 год с использованием комбинаций ключевых слов: patient-specific (пациент-специфичный), lattice (решётчатая структура), porous (пористый), TPMS, AM/3D printing (АП/3D-печать), segmental defect (сегментарный дефект), femur (бедренная кость), tibia (большеберцовая кость), reconstruction (реконструкция) и fixation methods (методы фиксации). Включались исследования, описывающие пациент-специфичные решётчатые/пористые имплантаты для реконструкции сегментарных дефектов бедренной или большеберцовой кости с достаточным уровнем детализации для классификации типа дефекта и концепции фиксации/интерфейса. Исключались работы, сосредоточенные исключительно на решётчатой структуре без контекста реконструкции имплантатом, или не содержащие ключевых сведений, необходимых для классификации. В случаях, когда несколько публикаций описывали перекрывающиеся случаи или одну серию имплантатов, в общих сводках двойной подсчёт не производился, а количественные данные извлекались из наиболее полного отчёта.
2. Типизация сегментарных дефектов и взаимодействие «имплантат–дефект»
Реконструкция сегментарных дефектов бедренной и большеберцовой костей охватывает несколько взаимосвязанных проектных областей: морфологию дефекта, стратегию фиксации, выбор материала, архитектуру решётчатой структуры и методы валидации. На Рис. 1 представлена эта многомерная структура и показано, как на PSLI влияют клинические концепции дефекта и имплантата, которые будут подробнее рассмотрены в подразделах, посвящённых типизации дефектов и воздействию имплантата.
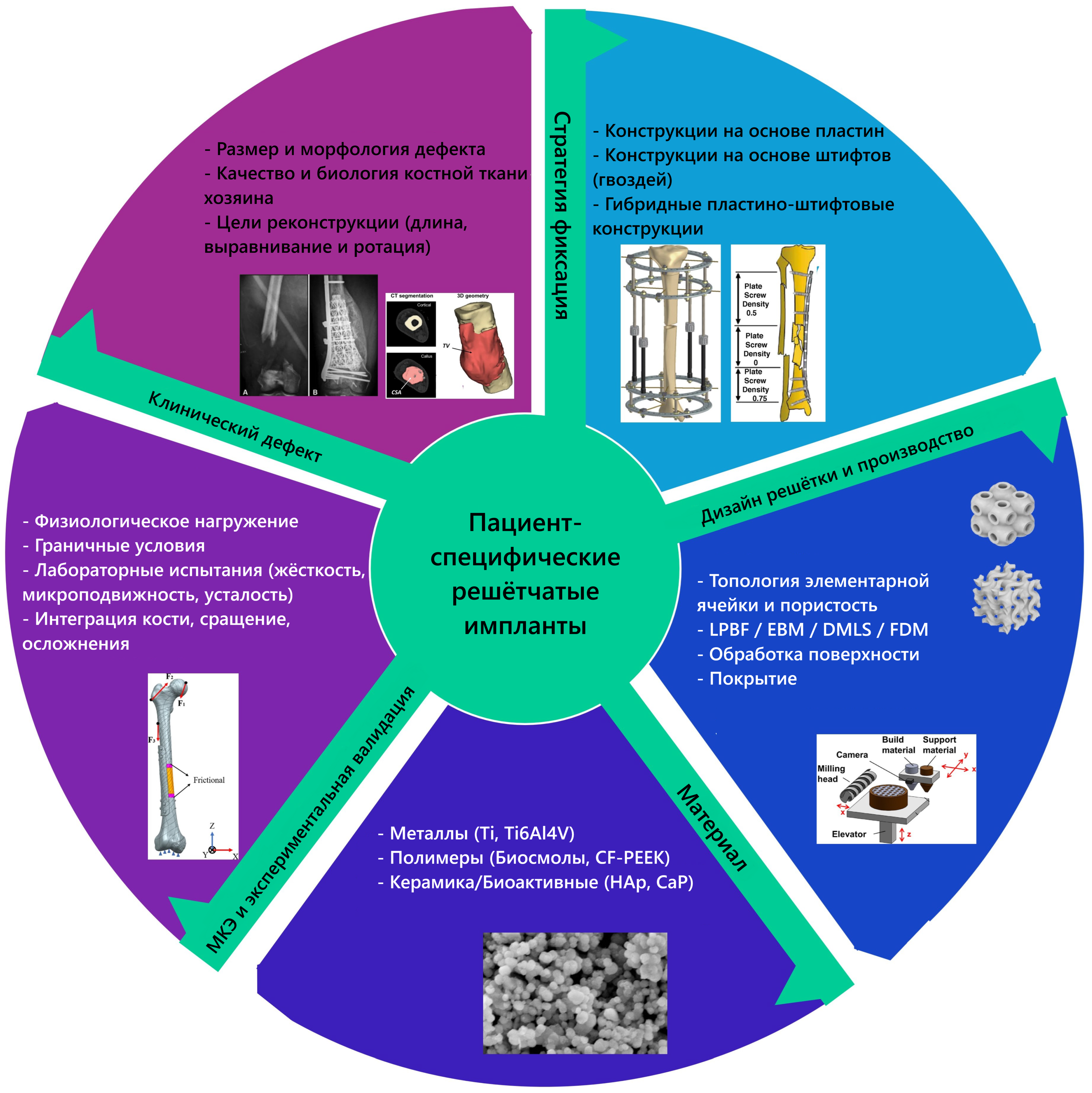
Рис. 1. Многодоменная структура для PSLI при реконструкции длинных трубчатых костей. Характеристика клинических дефектов по CT- и рентгенографическим данным и иллюстрации дефектов [17,18]. Примеры стратегий фиксации: конструкции на основе пластин, гвоздей и гибридные конструкции [19,20]. Микроструктуры материалов: металлические, полимерные и биоактивные керамические системы [21,22]. Рабочий процесс проектирования и изготовления решётчатых структур для архитектурированных скаффолдов, включая топологии элементарных ячеек и этапы АП [23,24,25]. Схемы FEM-верификации и экспериментальной валидации с физиологическим нагружением и стендовыми испытаниями [26,27]. В центральном круге показано, что PSLI находятся на пересечении этих пяти областей, а для достижения надёжных результатов необходимы согласованные решения во всех областях.
Типизация дефектов бедренной и большеберцовой костей: роль геометрии и размера
Сегментарные дефекты бедренной и большеберцовой костей могут различаться по исходам заживления. По данным рассмотренных исследований, исходы в наибольшей мере определяются морфологией дефекта и состоянием местной биологической среды (например, циркулярная потеря кости, поражение мягких тканей, инфекция). Анатомические факторы — поражённая кость и субрегиональная локализация — также могут влиять на осуществимость фиксации и заживление [28]. В проанализированных исследованиях применялся широкий спектр реконструктивных методик: аппарат Илизарова (костный транспорт), двухэтапная методика индуцированной мембраны Masquelet, васкуляризированные трансплантаты гребня подвздошной кости или малоберцовой кости, облучённые аутотрансплантаты и реконструкции с применением «алмазной концепции» [29]. Частота сращений существенно различалась в зависимости от метода [30]. При крупных и сложных дефектах сращение было достигнуто примерно в 50% случаев [28], тогда как при дефектах меньшего объёма с более благоприятной биологической средой наблюдалось полное сращение [28]. Сроки заживления значительно варьировали: от примерно 4 месяцев в отдельных случаях с высоким биологическим потенциалом трансплантата до более 18 месяцев при обширных дефектах, леченных поэтапным дистракционным остеогенезом [30]. Дефекты большего размера, прежде всего от 10 до 18 см, устойчиво ассоциировались с менее благоприятными исходами [31,32]: удлинением периода консолидации и повышенной частотой замедленного сращения или несращения [31]; в таких случаях нередко требовались дополнительные вмешательства. Помимо морфологии и факторов со стороны организма пациента, на исходы также влияла субрегиональная анатомия [33,34,35,36]. Характеристики дефекта играли ключевую роль в прогнозировании результатов заживления. Крупные дефекты с поражёнными мягкими тканями, инфекцией или предшествующими неудачными реконструкциями имели значительно сниженный потенциал заживления и более высокую частоту осложнений [37,38,39]. В подобных сложных случаях нередко требовались поэтапные или комбинированные реконструктивные стратегии для достижения оптимальной биологической и механической стабильности [40,41,42]. Вместе с тем потребность в повторных вмешательствах оставалась высокой — особенно в ситуациях с нарушением мягкотканевого покрова или хронической инфекцией [43,44]. В целом дефекты бедренной и большеберцовой костей демонстрируют схожие паттерны, поскольку большинство включённых исследований описывает результаты для бедренной кости, тогда как данные по большеберцовой кости представлены значительно скромнее и отражают иной биомеханический и мягкотканевый контекст [45].
На Рис. 2 представлена классификация сегментарных дефектов бедренной кости по размеру на малые (<2 см), промежуточные (2–5 см) и крупные (>5 см). Для каждого класса на рисунке приведены наиболее часто используемые методы реконструкции: от укорочения, цементной аугментации и костной пластики при малых дефектах до мультимодальных комбинаций васкуляризированных аутотрансплантатов, костного транспорта, дополнительного цемента и пациент-специфичных имплантатов при очень крупных дефектах. Группировка по размеру дефекта использовалась как практический способ структурирования литературы, а не как клиническое руководство, поскольку подходы к лечению и риски неблагоприятных исходов отчётливо меняются при превышении длины дефекта нескольких сантиметров, когда всё чаще возникают биологическое неблагополучие или поражение мягких тканей.
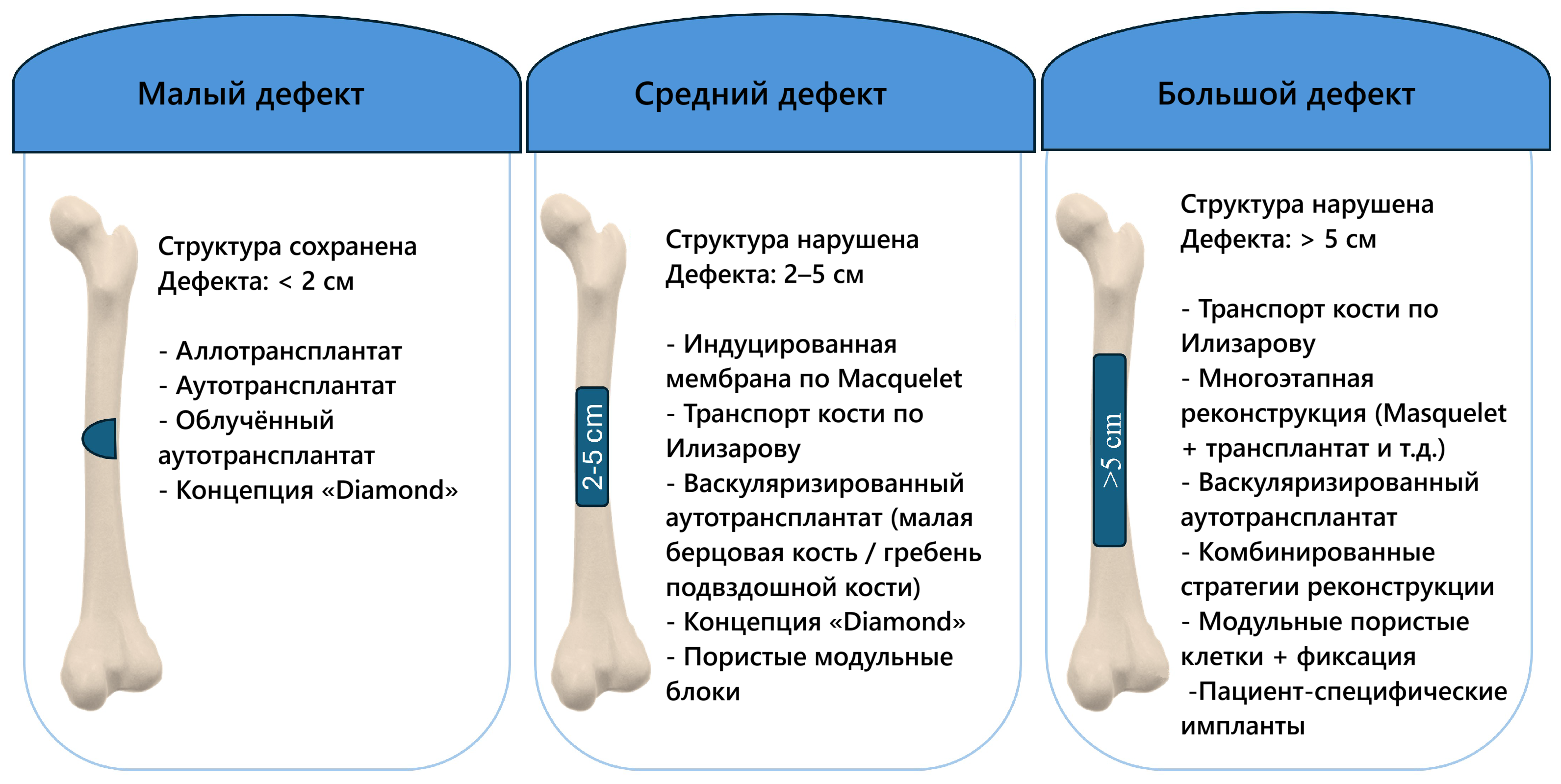
Рис. 2. Классификация сегментарных дефектов длинных трубчатых костей по размеру и соответствующие варианты реконструкции: малые дефекты < 2 см, промежуточные дефекты 2–5 см, крупные дефекты > 5 см.
Для дополнения концептуальной классификации по размеру, представленной на Рис. 2, в Рис. S1 (Дополнительные материалы) отражено распределение включённых исследований по классу размера дефекта и анатомическому субсегменту для ряда исследований, а в Рис. S2 (Дополнительные материалы) приведена блок-схема характеризации путей реконструкции сегментарных дефектов длинных трубчатых костей. Данное стратифицированное распределение выявляет характерное для литературы анатомическое смещение выборки: большинство включённых исследований посвящено дефектам бедренной кости (в особенности диафизарным), и в них преобладают крупные дефекты (>5 см), тогда как исследования сегментарных дефектов большеберцовой кости представлены в наборе данных крайне редко.
3. Стратегия фиксации, механическая среда и долговечность имплантата
Стратегия фиксации является ключевым фактором исходов заживления при дефектах длинных трубчатых костей, включая сегментарные и метафизарные дефекты бедренной и большеберцовой костей [46,47,48,49]. Данные клинических и биомеханических исследований неизменно свидетельствуют о том, что как выбор фиксирующей конструкции, так и её детальное механическое поведение принципиально важны для регенерации кости [50]. Традиционные методы фиксации — блокирующее пластинчатое остеосинтез, интрамедуллярный (IM) остеосинтез и кольцевая внешняя фиксация — существенно совершенствуются за счёт применения гибридных конфигураций (например, конструкций «гвоздь–пластина»), биологически ориентированных методик (в том числе методики Masquelet и костного транспорта) и новых конструкций пациент-специфичных или имплантируемых скаффолдов [51,52].
Для количественного и последовательного соотнесения механобиологии с конструктивными решениями в литературе по PSLI можно выделить пять повторяющихся механических характеристик: движение на уровне дефекта/щели (в мм), микроподвижность на границе раздела «имплантат–кость» (в мкм), локальные условия деформирования в кости/скаффолде (в процентах или микродеформациях), жёсткость конструкции и распределение нагрузки между фиксатором и скаффолдом (в Н/мм или кН/мм), а также радиологические прокси-показатели стабильности интерфейса (например, BIC/BII).
Среди рассмотренных исследований Liu et al. [24] сообщают, что относительное смещение более 150 мкм способствует формированию фиброзной ткани и угнетает костный рост; кроме того, авторы обсуждают деформацию на уровне скаффолда порядка 1–5% (при этом 1% отмечается как благоприятный уровень для раннего костеобразования) как условие, содействующее костеобразованию в пористых титановых скаффолдах. Используя аналогичный подход на основе механостата при анализе пациент-специфичного имплантата, Wong et al. [53] указывают пороговый уровень деформации повреждения примерно в 4000 мкε, выше которого микроповреждения могут задерживать сращение или приводить к несращению, и интерпретируют значения деформации на интерфейсе, преимущественно ниже этого порога, как благоприятные в непосредственном послеоперационном периоде, отмечая при этом ограничения макромасштабных FE-моделей для отражения микропористого интерфейса и последующей эволюции ткани [53]. Karuppudaiyan et al. [54] приводят величины смещения скаффолда 0,0031–0,012 мм по различным вариантам пористости (интактная бедренная кость: 0,002 мм) и напрямую связывают эти различия с микроподвижностью и снижением экранирования напряжений [54]. Entezari et al. [55] описывают, как жёсткое пластинчатое остеосинтез преимущественно переносит нагрузку через пластину, что может ограничивать нагрузку на скаффолд и создавать риск экранирования напряжений. Высокая энергия деформации указывает на избыточное движение, превышающее нормальные пределы, и подчёркивает необходимость баланса между потребностью в стабильных интерфейсах на ранних этапах для снижения микроподвижности и необходимостью передачи нагрузки на более поздних этапах для предотвращения устойчивого экранирования напряжений. Это объяснение согласуется с концепцией экранирования напряжений — понимаемого как снижение деформации и несоответствие в распределении жёсткости — в пользу пористых и/или градиентных по жёсткости стратегий [24,56]. В ряде исследований признаётся временная зависимость: врастание кости и ремоделирование способствуют постепенному повышению стабильности интерфейса, что ведёт к снижению микроподвижности на интерфейсе, которая в конечном счёте прекращается по мере улучшения стабильности [26,57]. Zhang et al. [57] также предложили принципы проектирования, ориентированные на достижение нулевой или минимальной микроподвижности по мере прогрессирования врастания кости — через управление пористостью, размером пор и формой стрежней — с акцентом на долгосрочную нагрузочную адаптацию, а не только на кратковременные характеристики.
Blázquez-Carmona et al. [18] изучали динамику распределения нагрузки и изменений жёсткости во времени и установили, что внешний фиксатор с жёсткостью Kf = 593 Н/мм в первые две недели воспринимал более 90% нагрузки; примерно через 30 дней происходило перераспределение нагрузки, при этом жёсткость костной мозоли возрастала с ~650 Н/мм на 40-й день примерно до 7 кН/мм к 60-му дню. Авторы также выявили переход к ремоделированию около 200-го дня. Pobloth et al. [58] непосредственно сравнивали различные режимы жёсткости фиксации: нагрузкораспределяющую пластину с жёсткостью ~555 Н/мм и экранирующую напряжения пластину с жёсткостью ~2857 Н/мм, а также жёсткость скаффолда в диапазоне 0,20–3,09 кН/мм; главные деформации на уровне пор составили ~0,23–0,6% в порах с аутотрансплантатом и ~0,65–1,3% в порах с костной мозолью. Авторы также рассматривали костеобразование внутри пористых имплантатов, указывая диапазон деформаций от 5% до 0,04% и уровень резорбции ниже 0,04% при конечно-элементных нагрузках 1372 Н в сжатии и 86 Н при изгибе. Chang et al. [27] аналогично использовали деформационный критерий, принимая 4000 мкε за верхнюю границу благоприятного костного роста вблизи интерфейса; измеренные деформации 2046–2253 мкε расценивались как способствующие росту кости, а результаты моделирования и эксперимента сравнивались количественно (например, 1752,6 против 1687,9 мкε; 2046,4 против 2133,7 мкε; 2252,57 против 2292,55 мкε); геометрические и материальные решения соотносились с экранированием напряжений и результатами остеоинтеграции (например, диаметр стержня 0,9 мм соответствовал модулю имплантата 14,99–15,88 ГПа и деформациям, превышающим 4000 мкε; модуль костного цемента 2,65 ГПа; внутрипросветное врастание > 79,8%).
Качество интерфейса может, однако, эффективно количественно оцениваться с помощью радиологических показателей и без непосредственного измерения микроподвижности. Obaton et al. [59] использовали опорный предел в 10 мкм (размер вокселя XCT — 6,8 мкм); сообщались значения контакта кости с имплантатом (BII = 3,3 мкм) и площадь контакта «кость–имплантат» (BIC = 95,4%, при норме 50–80%); несоответствие жёсткости (кортикальная кость 25–30 ГПа, сплав 38 ГПа) рассматривалось как фактор концентрации напряжений и экранирования напряжений.
Ряд исследований предоставляет количественные данные, преимущественно описывающие механический контекст без прямой механобиологической интерпретации. Это включает структурированные протоколы нагружения, такие как частичная нагрузка до 35 кг в течение 6 недель с последующим переходом к полной нагрузке в следующие 6 недель [17]. Описываемые скаффолды характеризуются пористостью до 82,7%, прочностью на сжатие от 1,76 до 9,34 МПа и структурными модулями от 52,2 до 212 МПа [60]. Описаны архитектуры с градиентом жёсткости: размер пор 500 мкм, пористость 84,22/77,68/68,45%, соответствующие модули 0,55/1,40/3,49 ГПа [61]. В других работах описывается экранирование напряжений через геометрические и нагрузочные определения без явного анализа микроподвижности: размеры ATS 8 × 8 × 5,8 мм, размеры стержней 200–500 мкм, пористость 50% и 62%, циклическое нагружение 150 Н, давление в FE-расчёте 1,25 МПа [62]. Кроме того, приводились показатели разрушения на печатных моделях бедренной кости: признаки трещинообразования при ~1,9% деформации и разрушение при 208,58 МПа и деформации 1,99% [63].
FE-анализ и экспериментальные исследования неизменно подтверждают, что оптимальная фиксация обеспечивает баланс между достаточной осевой и торсионной стабильностью и управляемой микроподвижностью, стимулирующей формирование костной мозоли [15,52,64,65]. Конструкции, обеспечивающие управляемое распределение нагрузки посредством гибких архитектур скаффолда, оптимизированных конфигураций пластин или комбинированных систем «гвоздь–пластина», создают более физиологичную механическую среду и в клинических случаях ассоциировались с более высокими показателями сращения и меньшим числом повторных операций [51,64,66,67]. Неадекватное согласование жёсткости конструкции с локальной механической средой может приводить к экранированию напряжений, прогрессирующей потере костной ткани и поздней асептической нестабильности; в то же время чрезмерно гибкие конструкции способны приводить к усталостному разрушению или нарушению заживления [68,69,70,71]. Эти данные подтверждают, что проектирование фиксации — это не только конструктивная, но и, по существу, биологическая задача: жёсткость конструкции и микроподвижность тесно связаны с дифференцировкой ткани, созреванием костной мозоли и долгосрочной функцией имплантата [58,72,73,74]. В непосредственном послеоперационном периоде реконструкции бедренной и большеберцовой костей успешно восстанавливают функцию по сравнению с дооперационным состоянием; однако сохраняющееся заметное отставание по сравнению с противоположной конечностью остаётся. Ранние показатели осложнений составляют около 3–7%; в структуре неудач чаще всего отмечаются перелом имплантата, прорезывание шурупа, перипротезный перелом, асептическое расшатывание и несращение [75,76,77]. Микроподвижность на интерфейсе «имплантат–кость» имеет ключевое значение для врастания кости: избыточная микроподвижность может приводить к формированию фиброзной ткани и расшатыванию, тогда как недостаточная — препятствовать остеоинтеграции и обусловливать долгосрочную нестабильность [78,79,80,81,82]. При длительном наблюдении несоответствие жёсткости и экранирование напряжений в значительной мере способствуют потере костной ткани, асептической нестабильности и перипротезным переломам. Напротив, использование низкомодульных или пористых/градиентных по жёсткости конструкций снижает перенос нагрузки на фиксирующее устройство, обеспечивая тем самым более равномерное нагружение кости-хозяина [83].
В Таблица 1 обобщены количественные метрики механобиологии, явно приведённые в отобранных исследованиях, с указанием механических показателей (например, деформация, микроподвижность, жёсткость и распределение нагрузки), их биологической интерпретации и соответствующих конструктивных рычагов. Полные сведения о приводимых метриках содержатся в Таблица S1 (Дополнительные материалы).
Таблица 1. Количественные показатели механобиологии, извлечённые из отобранных исследований; в каждой строке указаны приводимые метрики, их значения, биологическая интерпретация авторов и основные конструктивные рычаги.
| Год, Ссылка | Измеряемый показатель | Величина | Интерпретация + Конструктивный параметр |
| 2014, [61] | Пористость/геометрия с градиентом жёсткости | Поры 500 μm; стержни 120/170/230 μm; пористость 84,22/77,68/68,45%; модуль упругости 0,55/1,40/3,49 GPa | Тенденция передачи нагрузки в зависимости от жёсткости (качественная в тексте); подтверждает обоснование согласования жёсткости. |
| 2018, [58] | Жёсткость пластины; жёсткость каркаса; деформации на уровне пор; нагрузки методом конечных элементов | Пластина: 555 против 2857 N/mm; каркас: 0,20–3,09 kN/mm; деформации: 0,23–0,6% (поры аутотрансплантата), 0,65–1,3% (поры костной мозоли); приводимый диапазон формирования 5% до 0,04%, резорбция ниже ~0,04%; МКЭ: 1372 N сжатие, 86 N изгиб | Напрямую связывает жёсткость фиксации с условиями деформации (распределение нагрузки против экранирования напряжений) и диапазонами деформаций, значимыми для механобиологии. |
| 2018, [54] | Перемещение дефекта/конструкции (mm) | 0,0031–0,012 mm; интактная кость 0,002 mm | Используется для обсуждения относительного движения и снижения экранирования напряжений при различных конструкциях пористости. |
| 2019, [60] | Диапазоны пористости/прочности/модуля упругости | Пористость до 82,7%; прочность 1,76–9,34 MPa; модуль упругости 52,2–212 MPa | Механические диапазоны только для контекста; экранирование напряжений упоминается в общем виде (без величин микроподвижности/деформации). |
| 2019, [55] | Распределение нагрузки + обоснование через энергию деформации | Передача нагрузки описана качественно (доля нагрузки в % или жёсткость не приводятся) | Жёсткая пластина: основная нагрузка через пластину, ограниченная — через каркас (риск экранирования напряжений); высокая энергия деформации: избыточное движение за пределами физиологических значений; баланс стабильности и передачи нагрузки. |
| 2019, [17] | Время клинического протокола нагрузки | Частичная нагрузка на вес тела макс. 35 kg в течение 6 недель; постепенный переход к полной нагрузке в течение следующих 6 недель | Подтверждает изменяющуюся во времени механическую среду посредством протокола реабилитации (величины микроподвижности/деформации не приводятся). |
| 2020, [53] | Деформация на границе раздела (по типу механостата) | Пороговая деформация повреждения ~4000 με | Выше порога: риск микроповреждений, замедленное сращение/несращение; ниже: благоприятный показатель на ранней стадии; следует учитывать ограничения масштаба/моделирования. |
| 2021, [57] | Геометрия конструкции; пиковое напряжение по МКЭ; качественная оценка микроподвижности/времени | Поры 400–600 μm; стержни 240–320 μm; пористость 60–80%; пиковое напряжение 12,09 MPa; 1000 N, 3,09 MPa; 2000 N, 37,21 MPa; 3000 N | Микроподвижность/механическая стимуляция упоминаются, но не количественно оцениваются; микроподвижность уменьшается и исчезает со временем; отмечено экранирование напряжений со стороны пластины; пористая структура снижает экранирование. |
| 2021, [56] | Экранирование напряжений через распределение деформаций | Числовые величины не приводятся | Экранирование напряжений как снижение деформации; обосновывает согласование распределения жёсткости для получения профиля деформаций, близкого к интактной кости (значимо для ремоделирования). |
| 2022, [26] | Временна́я зависимость: врастание/ремоделирование | Описан зависящий от времени эффект (кривая μm/mm/время не приводится) | Врастание кости/ремоделирование повышают стабильность; долгосрочный стабильный комплекс «имплантат–кость». |
| 2023, [24] | Относительное перемещение на границе раздела; диапазон деформаций | Критическое перемещение 150 μm; деформация 1–5% (включая отметку ~1% на ранней стадии) | >150 μm: риск фиброзного сращения; 1–5% представлены как благоприятный диапазон в контексте данного пористого каркаса; подчёркивается стабильность и несоответствие жёсткости (экранирование напряжений). |
| 2023, [18] | Жёсткость фиксатора; эволюция распределения нагрузки; сроки ремоделирования | Kf = 593 N/mm; >90% усилия через фиксатор (первые две недели); инверсия после ~30 дней; жёсткость костной мозоли ~650 N/mm; на 40-й день до ~7 kN/mm примерно через 20 дней; переход к ремоделированию ~200 дней | Количественно описывает фазы ранней стабильности — передачи нагрузки — ремоделирования; обеспечивает разрешённую по времени механобиологию. |
| 2023, [59] | Прокси-показатели границы раздела на основе визуализации; несоответствие жёсткости | Референсный предел 10 μm; воксель/пиксель 6,8 μm; BII = 3,3 μm; BIC = 95,4%; кортикальная кость 25–30 GPa; титановый сплав 38 GPa | Количественно оценивает качество границы раздела (косвенный показатель стабильности) и связывает несоответствие жёсткости с концентрацией напряжений. |
| 2023, [62] | Геометрия + нагрузка/МКЭ (без микроподвижности) | 8 × 8 × 5,8 mm; стержни 200–500 μm; пористость 50% против 62%; циклическая нагрузка 150 N; давление по МКЭ 1,25 MPa | Описание несоответствия жёсткости/экранирования напряжений без приведения значений микроподвижности/движения щели/пороговых деформаций. |
| 2023, [63] | Деформация до разрушения (по модели) | Признаки разрушения при 1,9%; разрушение 208,58 MPa, деформация 1,99% | Не является работой по механорегуляции/врастанию; может использоваться лишь как контекст для ограниченных значений деформации. |
| 2024, [27] | Целевая деформация кости + валидация; чувствительность к параметрам конструкции | Максимальная деформация кости ≤ 4000 με; благоприятные деформации ~2046–2253 με; примеры: 1752,6 против 1687,9 με, 2046,4 против 2133,7 με, 2252,57 против 2292,55 με; диаметр стойки 0,9 mm → модуль упругости 14,99–15,88 GPa и деформация >4000 με; модуль упругости костного цемента 2,65 GPa; внутрипросветное врастание >79,8% | Использует ~4000 με как нежелательную верхнюю границу; связывает выбор геометрии/материала с результатами экранирования напряжений/остеоинтеграции. |
Приведённые данные подчёркивают взаимозависимость стратегии фиксации, механической среды и долговечности имплантата как ключевых целей проектирования. Кроме того, они демонстрируют необходимость стандартизированного отражения объёма движений (ROM), исходов, оценённых пациентом (PRO), осложнений и количественных механических метрик. Такая стандартизация является необходимым условием уточнения выбора конструкции и повышения долгосрочной выживаемости [72,73].
4. Анатомический и фиксационный контекст описанных имплантатов
Сегментарные дефекты длинных трубчатых костей возникают в различных анатомических локализациях с различной морфологией дефекта и состоянием кости-хозяина. Эти различия существенно влияют на проектирование, фиксацию и оценку пористых имплантатов. Длинный, циркулярный мета-диафизарный дефект дистального отдела бедренной кости предъявляет принципиально иные механические и биологические требования по сравнению с коротким диафизарным дефектом большеберцовой кости или стандартизированным дефектом в метатарзальной кости овцы, даже при одинаковой номинальной длине дефекта. Для сохранения клинической привязки обзора авторы вначале унифицируют описание когорт, источников визуализации, типов дефектов и стратегий фиксации по всей литературе [17,18,21,22,23,24,26,27,53,54,55,56,57,58,59,60,61,62,63,84,85,86,87,88,89,90], используя это как необходимый контекст для последующих разделов об архитектуре решётчатых структур, изготовлении и моделировании в настоящей Части I, а также более детально — в сопутствующей Части 2.
Таблица 2 содержит ключевые данные; полная таблица по исследованиям приведена в Дополнительной Таблице S1. Для каждого исследования указаны следующие сведения — кто, что, где и как: цель реконструкции (пациенты, мелкие или крупные животные или составные/трупные суррогаты), тип сегмента кости и архетип дефекта (диафизарный, метафизарный, мета-диафизарный; ограниченные или сегментарные/циркулярные дефекты; длина и морфология дефекта), а также источник получения анатомии и геометрии дефекта (клиническая CT, микро-CT, справочные наборы данных или синтетические модели). Фиксируется также выбранная концепция стабилизации и уровень трансляционной зрелости (чисто расчётный, стендовый, in vivo или клинический).
Таблица 2. Обзор анатомической локализации, архетипа дефекта, модели исследования, конвейера визуализации, класса фиксации и трансляционного статуса по включённым исследованиям дефектов длинных трубчатых костей.
| Ссылка, Год | Локализация | Архетип дефекта | Тип модели | Конвейер визуализации | Класс фиксации | Готовность |
| 2013, [84] | Дистальный диафиз бедренной кости | Сегментарный, 30 mm | Стендовые + МКЭ | КТ с картированием единиц Хаунсфилда | Латеральная блокируемая пластина | Стендовые и in silico |
| 2014, [61] | Средний диафиз бедренной кости | Сегментарный, 6 mm | Ex vivo (бедренные кости крысы) | Микро-КТ (архитектура имплантата) | Внутренняя блокируемая пластина из PEEK (RatFix) | Стендовые |
| 2015, [85] | Дистальный диафиз бедренной кости | Остеотомия, 5 mm | Только МКЭ | Без DICOM (публичная модель) | Ретроградный интрамедуллярный стержень + блокирующие элементы | In silico |
| 2018, [58], Случай 1 | Средний диафиз большеберцовой кости | Сегментарный дефект критического размера, 4 cm | In vivo (крупное животное) | Рентгенограммы + конечная визуализация | Фиксация пластиной (два варианта) | Доклинические in vivo |
| 2018, [58], Случай 2 | Бедренная кость и плечевая кость (клинические локализации) | Крупные сегментарные дефекты | Клиническая когорта | КТ-планирование + последующая визуализация | Пластинчатые конструкции с Ti-сетчатым каркасом | Клинические |
| 2018, [54] | Диафиз бедренной кости | Сегментарный (модельный), 8 mm | МКЭ и концептуальная валидация | КТ-сегментация (Mimics) | Без имплантатов фиксации | In silico |
| 2019, [55] | Среднее тело бедренной кости (композитное) | Сегментарный цилиндр, заполненный каркасом | Стендовые + МКЭ | Оптическое сканирование + DIC | Латеральная мыщелковая пластина | Стендовые и in silico |
| 2019, [22] | Типовой сегмент бедренной кости (не уточнён) | Без дефекта (исследование материала) | Стендовые (in vitro) | Без КТ (использован СЭМ) | Без имплантатов фиксации | Стендовые |
| 2019, [60] | Средний диафиз бедренной кости | Сегментарная модель (без патологии) | Стендовые (испытания изготовления) | КТ-сегментация (Mimics) | Без имплантатов фиксации | Стендовые |
| 2019, [17], (Пациент A) | Диафиз бедренной кости | Сегментарный, 15.2 cm | Клинический случай | КТ-планирование + рентгенограммы + контрольная КТ | Ti-клетка + интрамедуллярный стержень (Masquelet) | Клинические |
| 2019, [17], (Пациент B) | Метадиафиз бедренной кости | Сегментарный, 15.1 cm | Клинический случай | КТ-планирование + рентгенограммы + контрольная КТ | Ti-клетка + латеральная блокируемая пластина | Клинические |
| 2019, [17], (Пациент C) | Метадиафиз бедренной кости | Сегментарный, 18.4 cm | Клинический случай | КТ-планирование + рентгенограммы + контрольная КТ | Ti-клетка + латеральная блокируемая пластина | Клинические |
| 2019, [17], (Пациент D) | Метадиафиз бедренной кости | Сегментарный, 10.3 cm | Клинический случай | КТ-планирование + рентгенограммы + контрольная КТ | Ti-клетка + латеральная блокируемая пластина | Клинические |
| [17], 2019, (Пациент E) | Диафиз бедренной кости | Сегментарный, 11.1 cm | Клинический случай | КТ-планирование + рентгенограммы + контрольная КТ | Ti-клетка + интрамедуллярный стержень | Клинические |
| 2020, [86] | Средний диафиз бедренной кости (крыса) | Сегментарный, 3 mm | In vivo (крыса) | Рентген + микро-КТ | Блокируемая пластина из PEEK (RatFix) | Доклинические in vivo |
| 2020, [53] | Дистальная бедренная кость (область латерального мыщелка) | Крупный сегментарный дефект (травма) | Случай хирургического планирования | КТ-реконструкция | Пациентоспецифический имплантат + латеральная блокируемая пластина | In silico |
| 2021, [56] | Бедренная кость (секции полной модели) | Концепция замещения резекционного дефекта | Стендовые + МКЭ | КТ-сегментация (Mimics) | Без имплантатов фиксации (связанные в МКЭ) | Стендовые и in silico |
| 2021, [87] | Диафиз бедренной кости (крыса) | Сегментарный дефект критического размера, 8 mm | In vivo (крыса) | Рентген + микро-КТ | Фиксация пластиной через дефект | Доклинические in vivo |
| 2012, [21] | Типовая модель бедренной кости | Без явного дефекта (исследование каркаса) | Стендовые + МКЭ | Конвейер КТ-моделирования | Без имплантатов фиксации | Стендовые и in silico |
| 2021, [57], Случай 1 | Диафиз бедренной кости (человек) | Сегментарный, 11 cm | Клинический случай | Рентгенограммы (КТ не детализирована) | Пациентоспецифический имплантат + интрамедуллярный стержень | Клинические |
| 2021, [57], Случай 2 | Средний диафиз бедренной кости (овца) | Сегментарный дефект критического размера, 4 cm | In vivo (крупное животное) | Рентгенограммы + микро-КТ + МКЭ | Пластина и винты, интегрированные с имплантатом | Доклинические in vivo |
| 2021, [57], Случай 3 | Средний диафиз бедренной кости (овца) | Сегментарный дефект критического размера, 4 cm | In vivo (крупное животное) | Количественная оценка на основе микро-КТ | Пластина и винты, интегрированные с имплантатом | Доклинические in vivo |
| 2022, [23] | Бедренная кость (модельная) | Сегментарный дефект критического размера, 50 mm | Только МКЭ | КТ-сегментация | Без имплантатов фиксации | In silico |
| 2022, [26] | Дистальная латеральная бедренная кость | Крупный дефект (анатомически определённый) | Стендовые + МКЭ (композитные) | КТ пациента для определения размеров (детали не указаны) | Латеральная блокируемая пластина + винты | Стендовые и in silico |
| 2023, [24] | Бедренная кость (интеркалярная концепция) | Крупный сегментарный дефект (без числового значения) | Только МКЭ | КТ-сегментация (Mimics, Magics) | Интегрированное устройство фиксации (персонализированное) | In silico |
| 2023, [62] | Концептуальный (несколько локализаций показаны) | Модульные блоки (без единого дефекта) | Стендовые (in vitro + механические) | Микро-КТ (морфология каркаса) | Без имплантатов фиксации | Стендовые |
| 2023, [63] | Модель целой бедренной кости | Без дефекта (анатомическая модель) | Стендовые + МКЭ | КТ-сегментация | Без имплантатов фиксации | Стендовые |
| 2023, [18] | Плюсневая кость (овца) | Сегментарный, 15 mm | In vivo (крупное животное) | Предоперационная КТ + последующая визуализация | Внешний фиксатор (тип Илизарова) | Доклинические in vivo |
| [59], 2023 | Большеберцовая кость и плюсневая кость (овца) | Внутрикостные имплантаты (без сегментарного дефекта) | In vivo (крупное животное) | XCT после удаления имплантата + сегментация | Без имплантатов фиксации | Доклинические in vivo |
| [88], 2024 | Среднее тело большеберцовой кости (модель кролика) | Кортикальный дефект критического размера | Прототип + МКЭ | КТ-реконструкция | Изогнутая пластина + винты, интегрированные с клеткой | Стендовые и in silico |
| [89], 2024 | Тело бедренной кости | Крупные дефекты тела (два сценария) | Концепция прототипа | 2D медицинские изображения (рентген) | Интрамедуллярный стержень + модульные блоки | Стендовые |
| [27], 2024 | Дистальная бедренная кость | Модель дефекта 25 mm (плюс испытание на животных) | МКЭ + стендовые + in vivo | КТ и послеоперационная микро-КТ | Латеральная реконструктивная пластина + винты | Доклинические in vivo |
| [90], 2025 | Дистальная бедренная кость | Крупный дефект, 82 mm | Только МКЭ | КТ-сегментация | Каркас + соединительные пластины + винты | In silico |
В рамках этой схемы пациент-специфичные реконструкции бедренной и большеберцовой костей у людей составляют один основной подкласс. Lu et al. [90] и Benady et al. [91] проектируют индивидуализированные пористые Ti6Al4V-имплантаты непосредственно на CT-моделях длинных трубчатых костей и интегрируют их в пациент-специфичные хирургические рабочие процессы, тогда как Zhang et al. [57] совместно проектируют режущие направляющие, ножки и пористые сегменты для сложных мета-диафизарных реконструкций. Второй подкласс составляют доклинические модели диафизарных дефектов на мелких и крупных животных, где пористые цилиндры или сетки имплантируются в стандартизированные дефекты при контролируемом нагружении для оценки функции скаффолда и регенерации кости [57,87,88]. Третий подкласс включает методологические исследования и работы на составных костных моделях, где синтетические бедренные кости или биофиделичные суррогаты используются для калибровки FE-моделей, испытания конструкций «пластина–скаффолд» или изучения граничных условий в воспроизводимых условиях [21,84,92]. Работы по материалам — обработке поверхностей и покрытиям [56,93], а также более широкие обзоры пациент-специфичных FEM и практик моделирования [94,95] — обеспечивают дополнительный контекст в части коррозии, остеоинтеграции и стандартизации рабочих процессов. В различных классах конвейеры визуализации и моделирования в целом следуют единому алгоритму. Большинство клинических и доклинических исследований начинается с CT- или микро-CT DICOM-данных поражённой кости, которые при онкологических или инфекционных случаях иногда дополняются МРТ для уточнения границ резекции и отношений с мягкими тканями [57,90,91].
Стратегия фиксации и граничные условия фиксируются в обзоре, поскольку они определяют механическую среду, в которой функционирует решётчатая структура, и тем самым обусловливают интерпретацию распределения напряжений–деформаций, микроподвижности и рисков разрушения. В ряде работ с участием людей и на составных моделях бедренной кости анализируются открытопористые Ti-скаффолды в сочетании с боковыми блокирующими пластинами и винтами; при этом количественно оцениваются жёсткость конструкции, распределения напряжений и смещение суставной поверхности под нагрузкой, соответствующей фазе опоры [84,90]. Benady et al. [91] и Zhang et al. [57] сочетают индивидуализированные пористые сегменты с интрамедуллярными гвоздями, интегрированными ножками и/или пластинами, явно совместно проектируя имплантат, направляющие и фиксацию для восстановления оси, длины и конгруэнтности сустава при крупных сегментарных дефектах. В моделях на мелких и крупных животных фиксация нередко упрощается — применяются аппараты внешней фиксации, лёгкие пластины или в ряде случаев дополнительная фиксация отсутствует, — чтобы изолировать вклад жёсткости скаффолда, архитектуры пор и состава материала в регенерацию кости [87,88]. На другом полюсе находятся Shams et al. [21] и Baville et al. [92], которые намеренно используют идеализированные условия «без фиксации» или абстрактные граничные условия для прототипирования концепций решётчатых структур и сравнения формулировок с нагрузкой инерции облегчения versus пружинных или изостатических ограничений до их применения к более реалистичным конструкциям. Во всех этих примерах явно сформулированы допущения: сращённые интерфейсы «имплантат–кость», нагружение в фазе опоры или по данным походки, экспериментальная калибровка на составных образцах [84,90,91,92].
В Таблица 2 для каждого исследования указаны сегмент кости и тип дефекта, уровень когорты, подход к визуализации и сегментации, стратегия фиксации или концепция интерфейса «имплантат–кость», а также общая трансляционная зрелость. Данный обзор показывает, что в литературе преобладают модели диафиза бедренной кости и диафиза большеберцовой кости, тогда как подходы к визуализации и выбору фиксации существенно варьируют, что затрудняет прямое сравнение между исследованиями. Распределение фиксирующих конструкций по различным архетипам дефектов представлено на Рис. 3. В данном обзоре термин «стенд» обозначает стендовые лабораторные эксперименты, проводимые вне животных или пациентов (например, механические испытания, исследования на фантомах/костных эрзацах Sawbones или анализы in vitro). Термин «in silico» означает расчётные исследования, FE-анализы или численные конструктивные рабочие процессы.

Рис. 3. Представление стратегий фиксации по типам сегментарных дефектов длинных трубчатых костей. Горизонтальные полосы показывают число исследований, в которых отражается каждый тип дефекта; цветные и штриховые сегменты указывают на соответствующие применяемые категории фиксации.
Для дополнения качественного представления, приведённого на Рис. 3, количественными данными, в Рис. S3 (Дополнительные материалы) представлена частота стратегий фиксации в зависимости от комбинации «размер дефекта–анатомия», что основано на исследованиях, указанных в Таблица 1. В целом пластинчатые конструкции доминируют при большинстве рассматриваемых комбинаций, тогда как интрамедуллярные гвозди и гибридные стратегии «пластина–гвоздь» преимущественно встречаются при диафизарных реконструкциях бедренной кости, особенно при крупных дефектах. Для этой тепловой карты из анализа были исключены случаи, не связанные с реконструкцией сегментарных дефектов длинных трубчатых костей (например, модели без дефекта, исследования скаффолдов общего характера, внутрикостные имплантаты), а также случаи без чётко определённой фиксирующей конструкции.
Совокупность этих данных наглядно демонстрирует, как анатомический контекст и выбор фиксации определяют проектное пространство и возможность сопоставления результатов между исследованиями. Изучение Таблица 2 и Рис. 3 имеет практическое значение для интерпретации и проектирования пористых имплантатов. Во-первых, эффективность имплантата не следует обсуждать в отрыве от анатомической локализации, типа дефекта и стратегии фиксации, поскольку эти элементы совместно определяют механическую среду и задают контекст для интерпретации приводимых показателей напряжений, деформаций и микроподвижности. Во-вторых, разнообразие конвейеров визуализации, определений дефектов и фиксирующих конструкций означает, что сравнения между исследованиями наиболее информативны, когда результаты интерпретируются внутри чётко описанных подгрупп, а не в единой совокупности литературы. В перспективе это поддерживает более явную совместную логику проектирования, при которой выбор фиксации и архитектура имплантата определяются совместно для соответствия намеченной клинической цели, включая раннюю стабильность, управляемое распределение нагрузки и долгосрочную функциональность конструкции. Наконец, обзор подчёркивает необходимость последовательного описания геометрии дефекта, фиксирующей конструкции и принятых граничных условий, поскольку именно эти переменные определяют, допускают ли полученные результаты практический перевод в конструктивные правила.
5. Моделирование и архитектура решётчатых структур
Современная пористая ортопедия берёт начало в конце 1960-х — начале 1970-х годов, когда было установлено, что кость способна врастать в стабильные пористые металлические поверхности, обеспечивая бецементную долгосрочную фиксацию. Ранние технологии — плазменно-напылённый пористый титан, спечённые металловолоконные сетки и спечённые покрытия из кобальт-хромовых гранул — сформировали базовые принципы проектирования пористых поверхностей из CoCr и Ti для эндопротезов тазобедренного и коленного суставов [96,97,98]. Последующие обзоры убедительно обосновали, что данные покрытия снижают экранирование напряжений, повышают шероховатость поверхности и трение, а также обеспечивают надёжную остеоинтеграцию [97,99]. К началу–середине 1980-х годов ножки эндопротезов с пористым покрытием и бесцементные вертлужные компоненты для тотального эндопротезирования тазобедренного сустава (ТЭТС), а также анатомические коленные системы с пористым покрытием вошли в рутинную практику; Engh, Bobyn и другие авторы документально подтвердили врастание кости и роль прессовой посадки [100,101]. В конце 1990-х — 2000-х годах эти идеи получили развитие в форме трёхмерных пористых конструкций: метафизарных конусов из высокопористого тантала (trabecular metal), сочетающих высокую пористость, относительно низкую жёсткость и высокое трение для стабилизации крупных полостных и сегментарных дефектов метафизарной кости бедренной и большеберцовой костей при сложном ревизионном тотальном эндопротезировании коленного сустава (ТЭКС) [102,103].
От покрытий к несущим архитектурам с решётчатой структурой для реконструкции длинных трубчатых костей
Современная реконструкция длинных трубчатых костей эволюционировала от поверхностной пористости к передовым несущим решётчатым структурам с регулируемой проницаемостью. Решётчатые скаффолды, предназначенные для замещения дефектов длинных трубчатых костей — прежде всего бедренной и большеберцовой, — представляют собой структурированные пористые материалы с периодической или случайной геометрией [21,104,105,106,107,108]. Эти структуры разработаны для обеспечения механической поддержки как на кортикальном, так и на губчатом уровне, допуская при этом заполнение трансплантатом, васкуляризацию и остеоинтеграцию [107,108,109,110,111,112,113]. По сравнению со сплошными имплантатами архитектурированные решётчатые структуры снижают несоответствие жёсткостей «имплантат–кость» (уменьшая экранирование напряжений), создают большую поверхность с полностью взаимосвязанной пористостью для врастания тканей и могут быть адаптированы к анатомии пациента на основе CT-геометрии [23,26,56,73,104,114].
Архитектуры решётчатых структур, применяемые при реконструкции бедренной и большеберцовой костей, можно разделить на несколько обширных семейств. Сетчатые конструкции на основе стержней (Кельвин, ромбический додекаэдр, октет, соты, ромбик, «бриллиант») предлагают регулируемую механику — от растяжение-доминированной до изгиб-доминированной [21]: толщина балок и размер пор контролируют RD и жёсткость; такие конструкции просты в параметризации для АП и широко используются для согласования упругого модуля в костно-имитирующих решётчатых структурах [106,107,115,116]. Решётчатые структуры на основе триплоидных периодических минимальных поверхностей (TPMS) — гироид, примитив, «бриллиант» в листовой или скелетной форме — обеспечивают плавные, непрерывные поверхности с высокой удельной прочностью, регулируемой проницаемостью и средней кривизной, близкой к кости, снижая концентрацию напряжений и облегчая эвакуацию порошка [105,106,108,117]. Примитив-тип TPMS обычно демонстрирует более высокую проницаемость, тогда как гироид обеспечивает, как правило, бо́льшую удельную прочность; обе разновидности могут быть настроены на соответствие диапазонам жёсткости губчатой и кортикальной кости путём регулирования пористости и толщины стержня или листа [115,118,119]. Стохастические и архитектуры Вороного имитируют сложность и близкую к изотропной структуру губчатой кости, обеспечивают высокую проницаемость и часто применяются вокруг окон для трансплантата или гомогенизируются в FE-моделях для ускорения конструктивных итераций [109,112,113]. Топологически оптимизированные оболочки с решётчатыми окнами (нередко обозначаемые как поверхностно-решётчатые или сетчато-оконные имплантаты) сохраняют анатомическую оболочку для поддержки фиксации и суставной/контактной геометрии, открывая при этом крупные фенестрации, размещающие решётчатый наполнитель и измельчённый трансплантат, что снижает вес и увеличивает биологическую поверхность [26,114,120,121]. Функционально градиентные решётчатые структуры (FGL) вводят пространственные градиенты размера элементарной ячейки, относительной плотности или даже состава материала для следования распределению жёсткости кости, концентрации прочности в местах соединений или интерфейсов и достижения более физиологичной передачи нагрузки; пациент-специфичное градирование может быть получено непосредственно из HU-значений CT-данных [56,108,122,123,124].
В совокупности эти семейства решётчатых структур хорошо подходят для применения при реконструкции бедренной и большеберцовой костей, поскольку позволяют нацелить кажущийся модуль на кортикальный и губчатый диапазоны, сохраняя при этом адекватную прочность, обеспечивая проницаемость и поверхность для врастания тканей и перфузии трансплантата, повышая трение и шероховатость интерфейса (особенно при высокопористых тантал-подобных архитектурах) для немедленной стабильности, и поддаются изготовлению методами LPBF и EBM при клинически значимых размерах элементов. Кроме того, стратегии сглаживания геометрии (например, скругление, TPMS на основе листов) всё активнее применяются для снижения усталостно-критичных концентраций напряжений, что поддерживает долгосрочную надёжность, необходимую для несущих сегментарных реконструкций. Как обобщено на круговой диаграмме Рис. 4, большинство скаффолдов бедренной и большеберцовой костей в отобранных исследованиях сосредоточены на стержневых архитектурах (15/25 исследований, 60%). Остальные исследования распределяются по меньшим категориям: сплошные непористые конструкции (2/25, 8%) и гибридные оболочечно-решётчатые конструкции (2/25, 8%). Архитектуры, объединяющие несколько конструктивных семейств, встречаются редко и представлены только единичными исследованиями (по 1/25, 4%): TPMS и топологически оптимизированные, TPMS и гибридная оболочечно-решётчатая, гибридная оболочечно-решётчатая и поверхностная/сетчатая, стержневая и TPMS. Чисто TPMS-конструкции и чисто поверхностные/сетчатые конструкции также редки (по 1/25, 4%). В целом распределение свидетельствует о том, что реконструкции длинных трубчатых костей по-прежнему преимущественно опираются на традиционные стержневые решётчатые структуры, тогда как TPMS-концепции, гибридные и топологически-информированные подходы остаются сравнительно недостаточно представленными и только начинают появляться в приложениях к бедренной и большеберцовой костям.
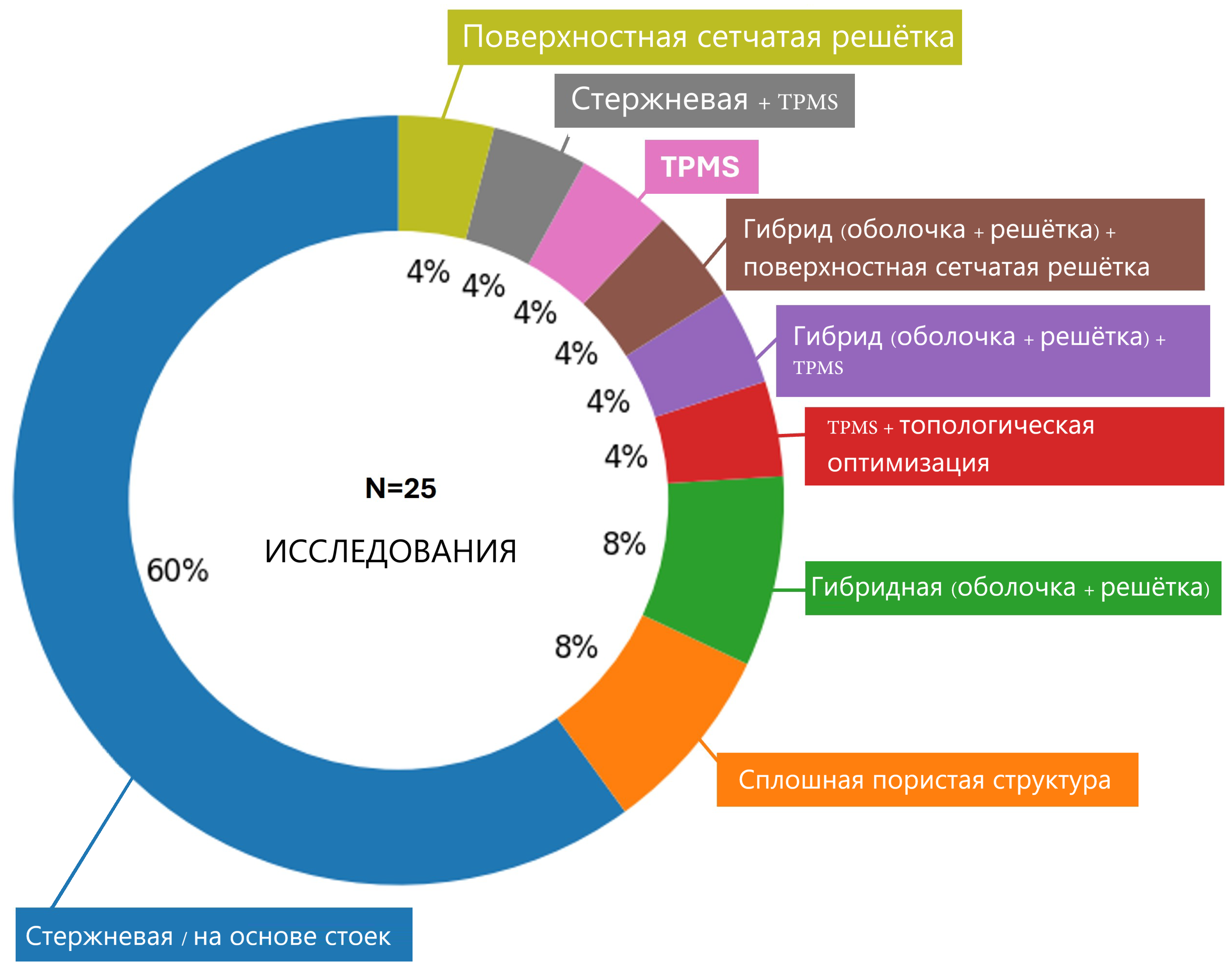
Рис. 4. Распределение семейств решётчатых структур в скаффолдах бедренной/большеберцовой костей по отобранным исследованиям [17,18,21,22,24,26,27,53,54,55,56,57,58,59,60,61,62,63,84,85,86,87,88,89,90].
Для дополнения обзора, основанного на подсчёте, Рис. 4 и Рис. S4 (Дополнительные материалы) обеспечивают полуколичественное сравнение доминирующих семейств решётчатых структур по механике, связанной с жёсткостью, отражению усталостной долговечности, морфологии, значимой для транспортировки (пористость/проницаемость), технологичности, ограничениям на размер элементов и управляемости конструкции — на основе параметров, явно приведённых в включённых исследованиях.
Распределение архитектур на Рис. 4 имеет значение как для практики проектирования, так и для интерпретации результатов сравнительных исследований. Преобладание стержневых решётчатых структур свидетельствует о том, что большая часть актуального конструктивного пространства формируется архитектурами, которые проще параметризовать, изготавливать и оценивать, что во многом объясняет их сохраняющееся лидерство в несущих реконструкциях. Вместе с тем ограниченное представительство TPMS-конструкций, гибридных оболочечно-решётчатых и топологически-информированных подходов означает, что в данной области ещё не выработаны чёткие правила выбора архитектуры в зависимости от клинической цели — ранней стабильности, долгосрочной надёжности или улучшения транспорта для интеграции трансплантата. Поэтому сравнения между исследованиями наиболее информативны, когда семейство решётчатых структур рассматривается как конструктивное решение с явным обоснованием, а выбранная архитектура обсуждается наряду с намеченной механической функцией, ожидаемым режимом разрушения и производственными ограничениями. В целом наблюдаемое распределение поддерживает более чёткое описание причин выбора конкретного семейства решётчатых структур и тех компромиссов по эффективности, которые оно призвано решать, — что позволяет перейти от каталогизации архитектур к переносимым принципам проектирования.
6. Материалы и аддитивное производство
Широкий спектр биоматериалов изучался для изготовления, при этом Ti-сплавы, главным образом Ti6Al4V (ELI с экстранизким содержанием O, N, C), являются основным материалом [17,26,53,56,57,58,61,62,84,87]; наряду с ними в отдельных работах встречаются чистый Ti [62] или другие Ti-сплавы [59,125]. Ti-сплавы преимущественно производились методом LPBF — нередко обозначаемым в включённых исследованиях как SLM или DMLS — и EBM [126,127,128]. Распределение материалов, применяемых в скаффолдах бедренной/большеберцовой костей на основе АП, обобщено на Рис. 5: Ti6Al4V является наиболее часто описываемым материалом (12/24 исследований, 48%), меньшая доля приходится на другие Ti-сплавы, полимеры, биокерамику [129] и рассасывающиеся композиты. На Рис. 6 представлено распределение производственных маршрутов: LPBF является наиболее часто описываемым процессом с долей 48%, тогда как экструзионное моделирование методом послойного наплавления (FDM), EBM и более специализированные методы — DMLS, роботизированное литьё или изготовление сеток — встречаются лишь в меньшинстве отчётов. Распределения материалов и процессов АП (Рис. 5 и Рис. 6) основаны на подмножестве исследований, явно указывающих материал и маршрут изготовления скаффолда (n = 24). Конструктивные и расчётные исследования без АП-построения ([85]) были исключены из этих распределений.
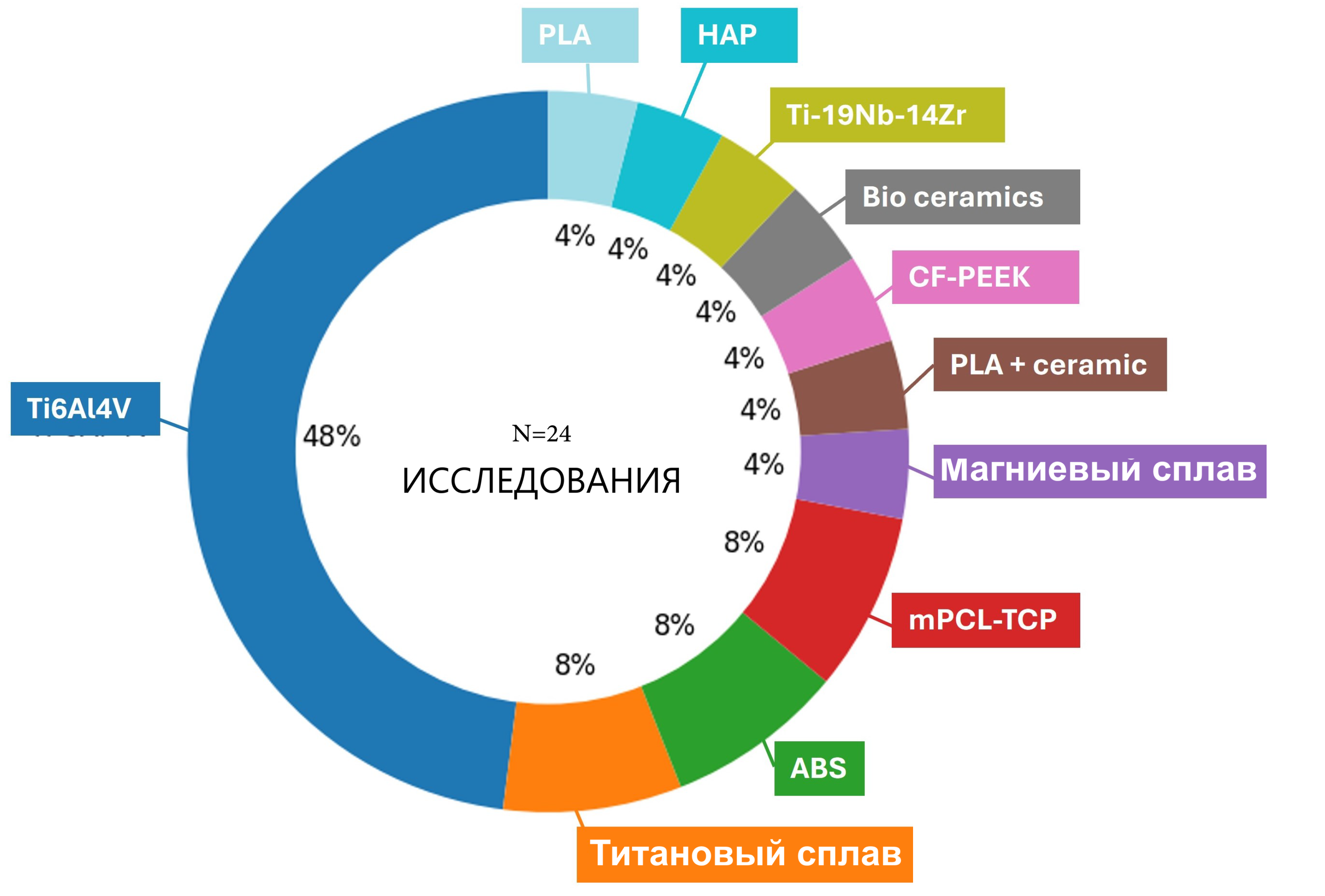
Рис. 5. Распределение материалов в скаффолдах бедренной/большеберцовой костей на основе АП по отобранным исследованиям [17,18,21,22,24,26,27,53,54,55,56,57,58,59,60,61,62,63,84,86,87,88,89,90].
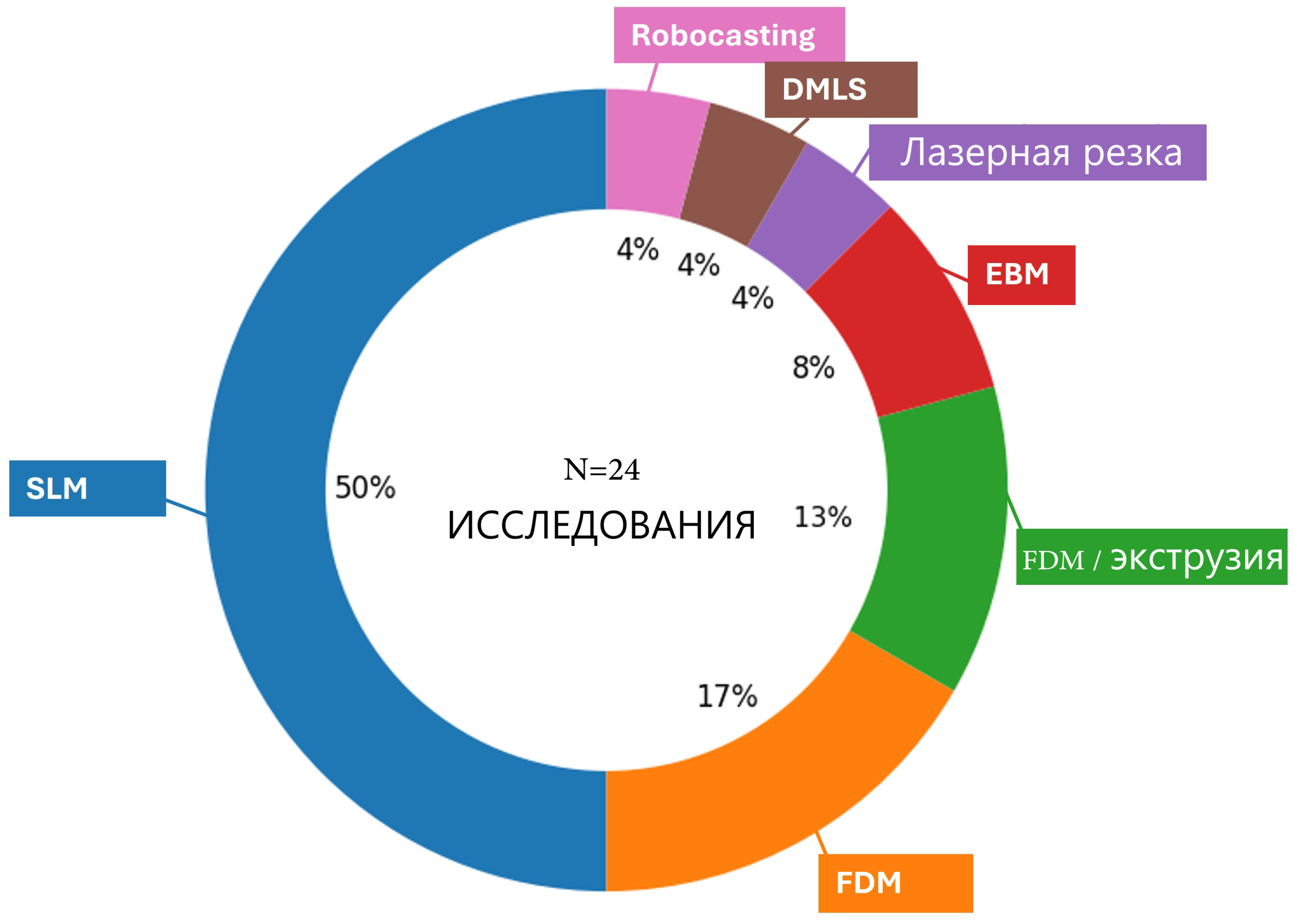
Рис. 6. Распределение методов АП по отобранным исследованиям [17,18,21,22,24,26,27,53,54,55,56,57,58,59,60,61,62,63,84,86,87,88,89,90].
Рис. 5 и Рис. 6 обобщают общие распределения материалов и маршрутов АП по включённым исследованиям; однако эти маргинальные распределения не раскрывают совместную встречаемость выбора материала и производственного маршрута в конкретных клинических контекстах. Для явного отражения этих взаимосвязей на Рис. 7 представлена диаграмма Сэнки, связывающая категорию дефекта, метод АП и материал (обозначенный как «mat» на рисунке) для исследований, включённых в дистрибутивный анализ. Визуализация демонстрирует явную концентрацию Ti6Al4V, производимого методами LPBF/EBM, при сегментарных реконструкциях и реконструкциях дистального отдела бедренной кости. Напротив, процессы на основе FDM/экструзии чаще сочетаются с полимерными/керамическими материалами в несегментарных или концептуально-ориентированных исследованиях.
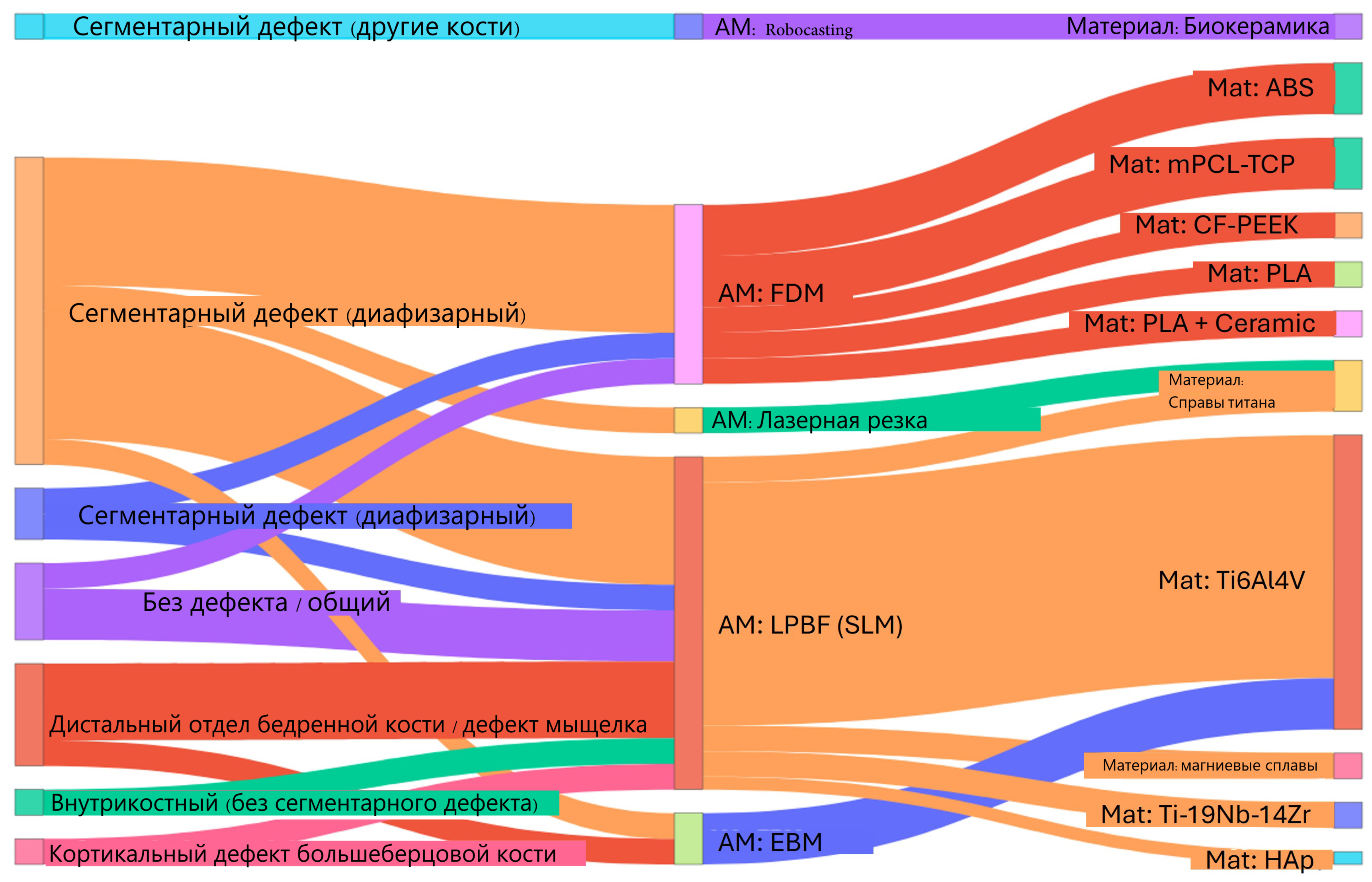
Рис. 7. Диаграмма Сэнки, связывающая тип дефекта, метод АП и материал в исследованиях скаффолдов бедренной/большеберцовой костей на основе АП [17,18,21,22,24,26,27,53,54,55,56,57,58,59,60,61,62,63,84,85,86,87,88,89,90].
Распределения материалов и АП на Рис. 5 и Рис. 6 вместе с ассоциациями, показанными на Рис. 7, формируют контекст, в котором показатели эффективности не могут быть отделены от производственных ограничений и этапов постобработки. Концентрация Ti6Al4V, производимого методами порошкового плавления, свидетельствует о том, что большая часть имеющихся данных привязана к паре материал–процесс, которая обеспечивает высокую геометрическую точность и клинически значимую прочность, однако при этом чувствительна к состоянию поверхности, внутренним дефектам и ограничениям по размерам элементов, что может влиять на усталостное поведение и остеоинтеграцию. Напротив, меньшая совокупность работ на основе полимеров, керамик и экструзии нередко отражает иные конструктивные цели и не должна рассматриваться как эквивалент металлических реконструкций с точки зрения несущих требований или долгосрочных ожиданий. Соответственно, будущие конструктивные решения должны рассматривать выбор материала и производственного маршрута как совместные детерминанты допустимой морфологии решётчатой структуры, характеристик поверхности и механической надёжности. Более последовательное описание производственных параметров и этапов постобработки также повысило бы интерпретируемость и воспроизводимость результатов между исследованиями. В этом смысле данные распределения носят не только описательный характер, но и указывают на то, что клиническая трансляция зависит от согласования клинической функции с технологически реализуемой архитектурой и надёжной производственной цепочкой.
7. Методологические обзоры: расчётные и экспериментальные исследования
В дополнение к обобщениям, ориентированным на анатомию, решётчатую структуру и производство, данный раздел реорганизует тот же массив работ по методологическим категориям. Вместо повторения сведений о локализации дефекта, архитектуре скаффолда, выборе материала или рабочем процессе персонализации, Таблица 3 содержит краткую сводную классификацию для каждой включённой статьи путём сочетания метки условий исследования с набором флагов методов. Метка условий исследования разграничивает клинические отчёты у людей (C), доклинические исследования in vivo на животных моделях (P-vivo) и доклинические исследования in vitro или ex vivo, такие как стендовые механические испытания, клеточные/тканевые анализы, суррогатные конструкции или трупные эксперименты (P-vitro/exvivo). Небольшое подмножество статей ограничено конструктивными/CAD-рабочими процессами без механических или биологических данных о результатах и соответственно отмечено в Таблица 3; когда условия исследования не поддаются определению по имеющимся сведениям, используется «(–)».
Таблица 3. Обзор методологического распределения включённых исследований.
| Год, Ссылка | Уровень доказательности | Флаги (S, E_mech, E_bio, V) |
| 2013, [84] | P-vitro/ex vivo | S + E_mech |
| 2014, [61] | P-vitro/ex vivo | S + E_mech |
| 2015, [85] | – | S |
| 2018, [58] | P-vivo | S + E_bio |
| 2018, [54] | – | S |
| 2019, [55] | P-vitro/ex vivo | S + E_mech + V |
| 2019, [22] | P-vitro/ex vivo | S + E_mech + E_bio. |
| 2019, [60] | P-vitro/ex vivo | E_mech |
| 2019, [17] | К + P-vitro/ex vivo | E_bio |
| 2020, [86] | P-vivo (+ ex vivo) | E_mech + E_bio |
| 2020, [53] | – | S |
| 2021, [56] | P-vitro/ex vivo | S + E_mech + V |
| 2021, [87] | P-vivo | E_mech + E_bio |
| 2021, [57] | К (человек) | E_bio |
| 2021, [21] | P-vitro/ex vivo | E_mech + S |
| 2022, [23] | – | S |
| 2022, [26] | P-vitro/ex vivo | S + E_mech + V |
| 2023, [24] | – | S |
| 2023, [62] | P-vivo/P-vitro | E_mech + E_bio |
| 2023, [63] | P-vitro/ex vivo | S + E_mech |
| 2023, [91] | К (человек), P-vitro/ex vivo | S + E_mech + E_bio |
| 2023, [18] | P-vivo | E_bio, E_mech |
| 2023, [59] | P-vivo | E_bio |
| 2024, [88] | P-vitro/ex vivo | S + E_mech |
| 2024, [89] | (только проектирование/САПР) | – |
| 2024, [92] | – | S |
| 2024, [27] | P-vivo + P-vitro/ex vivo | S + E_mech + E_bio + V |
| 2025, [90] | – | S |
Флаги метода обобщают содержание каждой статьи: моделирование или численное моделирование (S, включая конечно-элементный анализ), механические испытания (E_mech), биологические или клинические конечные точки (E_bio) и явное количественное сравнение результатов модели с измеренными данными (V). Флаг S не означает исключительно расчётное исследование; он лишь указывает, что численное моделирование присутствует, и может встречаться как самостоятельно, так и совместно с экспериментами. E_mech включает стендовые или ex vivo испытания: квазистатические или циклические испытания, испытания на изгиб или кручение. E_bio применяется при наличии биологических или клинических результатов (например, данных о заживлении/регенерации in vivo, гистологии, морфометрии на основе микро-CT, контакте кости с имплантатом или результатах наблюдения за пациентами). V зарезервирован для исследований, обеспечивающих явное количественное сравнение модели и измерений (например, предсказанной и измеренной деформации, жёсткости, распределения нагрузки или движения конструкции). Поскольку многие статьи используют гибридные конвейеры, исследования нередко несут комбинации флагов (например, S + E_mech или S + E_mech + E_bio + V). Рис. 8 обобщает распределение флагов методов по включённым исследованиям и подчёркивает преобладание моделирования и механических испытаний над биологически-закреплёнными и количественно-валидированными работами.
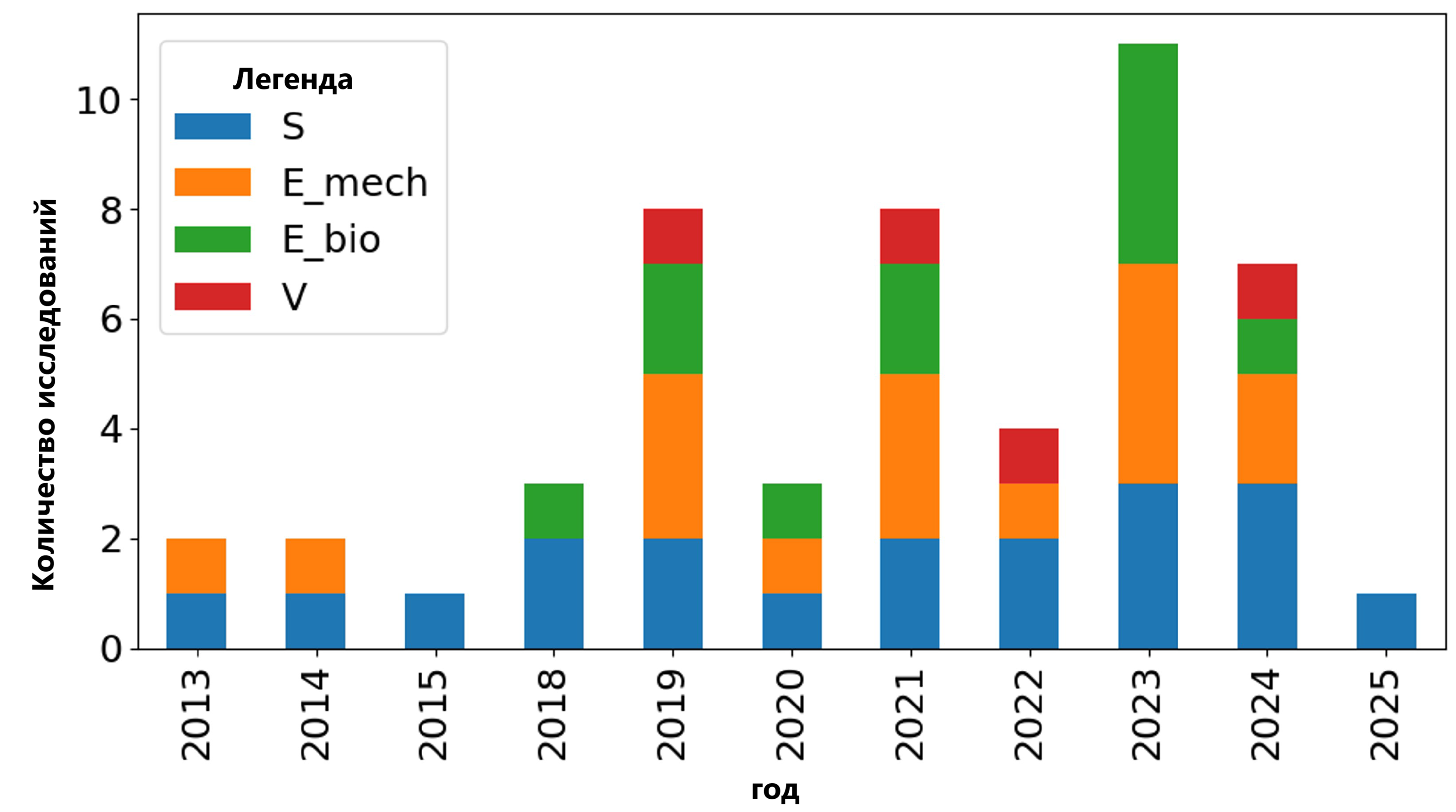
Рис. 8. Временно́е распределение применявшихся методов по включённым исследованиям. Накопленные полосы показывают число статей, в которых отражено моделирование (S), механические испытания (E_mech), биологические или клинические конечные точки (E_bio) и количественное сравнение модели и измерений (V); одно исследование может вносить вклад в несколько категорий [17,18,21,22,24,26,27,53,54,55,56,57,58,59,60,61,62,63,84,86,87,88,89,90].
7.1. Обзор расчётных и численных методов моделирования
FE-моделирование является основным инструментом анализа передачи нагрузки, механики фиксации и риска разрушения длинных трубчатых костей — прежде всего бедренной и большеберцовой. Типичные модели охватывают спектр от идеализированных кортикально-губчатых диафизов и суррогатных дефектов до полностью пациент-специфичных геометрий, построенных на CT-данных [56,63,84,85,90]. В зависимости от задачи исследования анализы охватывают осевое сжатие, изгиб и кручение или прогнозируют напряжения и деформации при физиологическом нагружении, стоянии на одной ноге и нагрузках по данным походки, с реакциями суставов и основными группами мышц, приложенными в области тазобедренного или коленного сустава, и ограничениями в дистальном отделе бедренной кости или проксимальном/дистальном отделе большеберцовой кости [26,27,84,85]. Также используются полные модели бедренной кости с переменными упругими свойствами, определяемыми на основе числа Хаунсфилда (HU), для изучения интрамедуллярных гвоздей, пластин и имплантатов при таких видах активности, как стояние на одной ноге или ходьба [85,92]. Более широкое обсуждение задач, характерных для пациент-специфичного моделирования, см. в [95]. При реконструкции сегментарных дефектов моделирование применяется для сравнения архитектур скаффолдов, оценки конфигураций пластин или гвоздей, а также количественного описания экранирования напряжений, микроподвижности и усталостно-критичных зон как в имплантате, так и в кости-хозяине [23,26,27,58]. Более продвинутые алгоритмы включают картирование плотности–упругости на основе CT, регионально градиентные материалы или механобиологические критерии для управления настройкой жёсткости и, в ряде случаев, прогнозирования тенденций дифференцировки тканей с течением времени [56,58,90]. В совокупности эти подходы формируют широко применяемый инструментарий для виртуальных испытаний реконструкций длинных трубчатых костей до стендовой или прижизненной проверки.
Среди ранних работ — оценка конструкций «скаффолд–пластина» для дистального отдела бедренной кости при физиологических нагрузках в тазобедренном суставе и мышечных нагрузках [84], анализ чувствительности граничных условий для ретроградного интрамедуллярного остеосинтеза [85] и механобиологически направленная оптимизация конструкций «пластина–скаффолд» при дефектах большеберцовой кости овцы [58]. Более поздние работы охватывают диапазон от сравнений TPMS на уровне элементарной ячейки и скаффолда [22,23] до сегментов бедренной кости с картированием жёсткости на основе CT и регионально настроенными пористыми имплантатами [56], топологически оптимизированных или решётчатых реконструкций дистального отдела бедренной кости [26,27] и крупных пациент-специфичных дефектов бедренной кости с альтернативными конструкциями «скаффолд–пластина–винт» [90]. Ключевые различия между моделями заключаются в геометрической сложности (только решётчатая структура против полной конструкции «кость–имплантат»), представлении материалов (однородное против CT-картированного по плотности; линейно-упругое против более сложных конститутивных моделей) и граничных/нагрузочных условиях (упрощённое одноосное сжатие против многоосного, физиологически обоснованного нагружения по данным походки).
По всей включённой литературе FE-моделирование применяется преимущественно как сравнительный инструмент для скрининга концепций реконструкции длинных трубчатых костей до или параллельно со стендовой и доклинической проверкой. Большинство исследований строят конструкции бедренной/большеберцовой кости с упрощёнными, преимущественно линейно-упругими описаниями материалов и затем оценивают, как архитектура имплантата и стратегия фиксации формируют передачу нагрузки, распределения напряжений/деформаций, жёсткость конструкции и межфрагментарное движение при идеализированном представлении нагружения при опоре на ногу (нередко нагружение при стоянии на одной ноге или с вдохновлёнными данными походки нагрузками и дистальными ограничениями) [23,24,26,53,58,84,85,90]. Хотя конкретные граничные условия и определения интерфейсов существенно различаются между статьями и могут существенно смещать прогнозируемые паттерны напряжений и тенденции жёсткости [85,92], FE-результаты неизменно используются для формулирования конструктивных компромиссов: чаще всего баланс между пористостью/проницаемостью и механической стабильностью [23,54,84] или между согласованием жёсткости и экранированием напряжений [24,56,58]. Важно, что ряд исследований выходит за рамки расчётного отражения: параметры материалов калибруются по данным механической характеризации или прогнозы модели количественно сопоставляются с измеренными полями жёсткости/деформаций в блоках скаффолда или на уровне конструкции [22,26,27,55,56,57,63,88]. В связи с этим результаты FE рассматриваются преимущественно как доказательство сравнительного позиционирования и понимания механизмов, тогда как специфичные для исследования конструктивные допущения, упрощения и статус валидации подробно задокументированы в Части 2.
7.2. Экспериментальный обзор: механические испытания
В экспериментальных условиях реконструктивные оценки длинных трубчатых костей проводятся либо на отдельных образцах скаффолдов, либо на конструкциях «кость–имплантат», установленных в суррогатных или трупных сегментах. Стендовая характеризация напечатанных архитектур обычно начинается с одноосного сжатия (реже — с вдавливания или комбинированного нагружения) для количественного определения кажущейся жёсткости, прочности и поглощения энергии и для оказания помощи в калибровке материалов для последующих анализов на уровне конструкции [22,55,56,84,88]. В контексте конструкций многие исследования прикрепляют сегменты бедренной кости с дефектом (синтетические или трупные) к системам «пластина–скаффолд» или имплантатам, используя квазистатическое осевое сжатие или сочетание сжатия и изгиба для имитации нагружения при опоре на ногу. Типичные измерения включают общую жёсткость конструкции, распределение нагрузки и относительное движение в зоне дефекта [26,55,61]. Ряд исследований расширяет механическую оценку за пределы простого нагружения, включая циклические испытания или оценку торсионной прочности для исследования долговечности и ротационной стабильности — особенно при доклинических оценках после заживления [62,87]. В целом эти эксперименты обеспечивают значимую оценку осуществимости и сравнительной стабильности; однако они нередко проводятся при упрощённых граничных условиях и ограниченных сценариях нагружения, которые могут не в полной мере отражать многонаправленные и усталостно-обусловленные требования повседневной деятельности. В дополнение к моделям с составными костями и трупными материалами доклинические исследования предоставляют биологические данные при принципиальной зависимости от контролируемых или упрощённых механических условий. Прижизненные модели на животных связывают архитектуру имплантата и стратегию фиксации с костеобразованием и интеграцией, оцениваемыми методами рентгенографии, микро-CT, гистологии и в ряде случаев ex vivo механических испытаний эксплантированных сегментов [18,27,59,86,87]. Альтернативные суррогатные методы, такие как костные эрзацы из FDM-напечатанного полиуретана или полиамида, применялись для воспроизводимой оценки механики конструкции без ограничений на варианты, присущих трупным материалам [55,63].
7.3. Ограничения базы исследований
По всем включённым исследованиям надёжность выводов существенно зависит от условий исследования и испытаний. Механические испытания обеспечивают прямую оценку жёсткости и прочности конструкции; однако они нередко опираются на упрощённые условия нагружения, короткие периоды испытания и суррогатные субстраты или приспособления, не отражающие полный диапазон многонаправленных и усталостных нагрузок повседневной жизни. Доклинические исследования in vivo дают представление о биологических реакциях и врастании кости; однако результаты могут существенно варьировать в зависимости от вида животного, размера дефекта, метода фиксации и продолжительности наблюдения. Поэтому при переносе этих данных на реконструкцию длинных трубчатых костей у взрослых людей необходима осторожность. Клинические отчёты обеспечивают наиболее прямое подтверждение осуществимости при реальных показаниях, однако их количество остаётся ограниченным, и они, как правило, представляют небольшие серии без группы сравнения. В целом базу исследований доминируют моделирование и стендовые испытания, тогда как длительное наблюдение, усталостно-ориентированные протоколы, крупные клинические когорты и последовательные количественные сравнения «модель–измерение» относительно редки.
В совокупности Таблица 3 и Рис. 8 отражают распределение включённых статей по моделированию (S), механическим испытаниям (E_mech), биологическим или клиническим конечным точкам (E_bio) и явному количественному сравнению «модель–измерение» (V). Распределение показывает преобладание численных исследований и стендовых механических испытаний при меньшем числе работ, сообщающих о биологическом наблюдении или количественной валидации, что означает: реконструкции длинных трубчатых костей с решётчатой структурой пока подкреплены преимущественно расчётными и экспериментально-стендовыми данными. Это имеет два следствия для синтеза и принятия решений: во-первых, данные расчётно-ориентированных исследований или кратковременных механических испытаний следует интерпретировать как сравнительное руководство для выбора конструкции и выявления рисков, а не как прямые предикторы клинической эффективности; во-вторых, ограниченная связь между результатами моделирования, измеренным поведением конструкции и биологической интеграцией подчёркивает необходимость более тесной интеграции моделирования, механических испытаний и конечных точек наблюдения в рамках единого рабочего процесса. В следующих подразделах (и в сопутствующем клиническом обзоре Часть 2) данное кодирование используется для противопоставления допущений моделирования и экспериментальных условий, а также для выделения повторяющихся пробелов: упрощённое нагружение, ограниченный учёт зависящего от времени ремоделирования и усталости, редкое биологическое наблюдение и практически полное отсутствие систематического анализа неопределённостей.
8. Проблемы и перспективные направления
Несмотря на значительные успехи в области CT-планирования, пациент-специфичных конструкций и модульной пористой реконструкции, ряд проблем требует решения в следующих аспектах: клинический и дефект-ориентированный контекст, фиксация и механическая среда, анатомо-фиксационные регистры, архитектура решётчатых структур, материалы и АП, а также методологические конвейеры. Устранение этих пробелов является необходимым условием перехода архитектурированных скаффолдов от технически впечатляющих единичных наблюдений к воспроизводимым стратегиям лечения.
С клинической точки зрения доказательная база в поддержку данных подходов расширяется. Дефект-ориентированные дескрипторы (размер, локализация, морфология, биология хозяина, статус инфекции) приводятся непоследовательно, что ограничивает возможности мета-анализа и осложняет установление показаний различными методами. Сроки наблюдения нередко кратковременны, а долгосрочные данные выживаемости для крупных сегментарных дефектов, реконструируемых пористыми скаффолдами, остаются скудными в сравнении с более устоявшимися методами — костным транспортом или мегапротезами. Перспективные работы должны быть сосредоточены на стратифицированных по дефектам регистрах с унифицированными классификациями, протоколами визуализации и функциональными показателями и исходами, оценёнными пациентом, — в идеале охватывающих несколько центров и стратегий реконструкции. Такие наборы данных необходимы для определения допустимых границ размера дефекта для различных концепций имплантатов, количественного описания паттернов осложнений в группах высокого риска и создания доказательных рекомендаций вместо экспертного мнения.
Фиксация остаётся основным источником вариабельности. В клинических, доклинических и расчётных исследованиях пластины, гвозди, аппараты внешней фиксации, гибридные конструкции и фиксация, интегрированная в скаффолд, применяются при весьма различных профилях жёсткости и граничных условиях, нередко без систематического сравнения. Краткосрочная стабильность обычно документируется, однако долгосрочная эволюция жёсткости конструкции, экранирования напряжений и качества перипротезной кости редко отслеживается стандартизированным образом. Перспективные работы должны рассматривать стратегию фиксации, конструкцию скаффолда и протокол реабилитации как взаимосвязанную систему: оптимизацию конструкции на уровне конструкции с нацеливанием на деформационные окна, благоприятные для регенерации; явное описание режимов нагружения; и по возможности механический мониторинг (например, инструментированные фиксаторы или серийные измерения жёсткости). Параллельно необходимы более надёжные данные по усталости и устойчивости к повреждениям как для скаффолдов, так и для фиксирующего оборудования в конкретных условиях нагружения, создаваемых дефектами длинных трубчатых костей.
Анатомо-фиксационный регистр настоящего обзора выявляет, насколько сильно исходы зависят от архетипа дефекта и контекста кости-хозяина, но также обнажает пробелы. Ряд клинически важных сценариев — очень длинные диафизарные дефекты, многосегментарные мета-диафизарные дефекты, периартикулярная потеря кости в сочетании с недостаточностью связочного аппарата — по-прежнему представлен преимущественно единичными наблюдениями или чисто расчётными моделями. Дефекты большеберцовой кости, детские случаи и пациенты с остеопорозом представлены значительно хуже по сравнению с взрослыми моделями диафиза бедренной кости. Ключевым перспективным направлением является формирование структурированных наборов данных, охватывающих возрастные группы, сегменты костей и этиологии и фиксирующих не только выбор имплантата и фиксации, но и временну́ю визуализацию, биологические дополнения и пути повторных операций. Такие наборы данных могут стать основой для инструментов поддержки принятия решений, предлагающих семейства конструкций и шаблоны скаффолдов, адаптированные к паттерну дефекта и факторам, специфичным для пациента.
На конструктивном уровне лишь небольшая часть доступного пространства решётчатых и градиентных конструкций исследована применительно к реконструкции длинных трубчатых костей. Большинство работ опираются на ограниченный набор семейств элементарных ячеек и относительно простые схемы градирования, как правило, настроенные на кажущуюся жёсткость и в меньшей мере — на проницаемость. Мультимасштабные иерархические архитектуры, сочетающие кортикальные нагрузочные пути с губчатоподобными внутренними структурами или объединяющие различные семейства решётчатых структур в одном имплантате, в основном остаются на концептуальном, а не на валидированном уровне. Также практически отсутствует количественное руководство по компромиссам между механической надёжностью, проницаемостью, площадью поверхности для трансплантата и врастания, а также технологичностью. Поэтому будущие исследования должны быть нацелены на разработку систематических конструктивных карт, интегрирующих эксперименты, FEA и механобиологические модели для соотнесения типа дефекта и схемы фиксации с рекомендуемыми семействами решётчатых структур, диапазонами пористости, градиентами и окнами для трансплантата. Оптимизационные алгоритмы, способные предлагать и ранжировать архитектуры с учётом клинических и производственных ограничений, являются естественным следующим шагом.
Материалы и процессы АП ставят собственные задачи. Для металлических решётчатых структур усталостное поведение при смешанном нагружении, влияние состояния поверхности и постобработки на долгосрочные характеристики и последствия продуктов износа/коррозии в конструкциях с большой площадью поверхности охарактеризованы недостаточно. Полимерно-керамические и биорассасывающиеся решётчатые структуры, привлекательные для молодых пациентов и концепций скаффолд-направляемой регенерации кости, ставят открытые вопросы в отношении кинетики деградации, изменяющихся механических свойств и взаимодействия между резорбцией, фиксацией и костеобразованием в несущих сегментах. Для всех материалов необходимы надёжные, клинически совместимые системы обеспечения качества, связывающие параметры АП-процесса и контроль in-process с механическими и проницаемостными характеристиками на уровне скаффолда. Перспективные работы должны быть сосредоточены на определении допусков для размера пор, связности и шероховатости поверхности; интеграции неразрушающего контроля в АП-рабочие процессы; и разработке стратегий смешанных материалов (например, Ti-оболочки с рассасывающимися сердечниками), пригодных для регуляторного утверждения.
С методологической точки зрения расчётные и стендовые конвейеры мощны, но далеки от гармонизации. FE-модели существенно различаются по практике сегментации, картированию «плотность–упругость», законам материалов и граничным условиям, что затрудняет сравнение результатов между исследованиями или их повторное использование в регуляторных контекстах. Экспериментальные работы нередко сосредоточены на квазистатических испытаниях изолированных скаффолдов или упрощённых конструкций при относительно малом внимании к усталости, многоосному нагружению или зависящему от времени ремоделированию. Биологические данные (как in vitro, так и in vivo) также неоднородны по виду животных, моделям дефектов и метрикам результатов.
Важными шагами вперёд являются: согласование общих эталонных геометрий и сценариев нагружения для дефектов длинных трубчатых костей; определение минимальных стандартов отчётности для FE-моделирования и механических испытаний; регулярное включение анализа неопределённостей и чувствительности в конструктивные исследования; более тесная увязка механобиологических моделей с продольными доклиническими данными для перехода от краткосрочных механических суррогатов к истинным результатам заживления. В долгосрочной перспективе виртуальные когорты и расчётные клинические испытания, объединяющие библиотеки CT пациентов с валидированными FE-конвейерами, могли бы снизить риски новых концепций скаффолдов до их клинического применения.
Наконец, существующие рабочие процессы «от визуализации к имплантату» остаются трудоёмкими и центро-специфичными. Сегментация, проектирование решётчатых структур, оптимизация конструкции и подготовка к печати обычно выполняются в нескольких программных платформах специалистами, при этом регуляторные пути и неформальное обеспечение качества разрабатываются для каждого случая индивидуально. Это ограничивает масштабируемость и затрудняет воспроизведение перспективных рабочих процессов в других клиниках. Перспективные работы должны быть нацелены на совместимые конвейеры PACS–планирование–FEM–АП со встроенными AI-инструментами для сегментации, определения ориентиров и автоматического предложения шаблонов имплантата/фиксации; полуавтоматической верификацией с заранее определёнными механическими и анатомическими ограничениями; и структурированным экспортом данных о конструкции и валидации для регуляторного представления. Подобные конвейеры сократят время проектирования, уменьшат зависимость от оператора и сделают сложные концепции решётчатых структур и смешанных материалов доступными за пределами нескольких специализированных центров.
В качестве обобщения соответствия дескрипторов дефекта (размер, морфология, статус инфекции) и факторов хозяина (качество кости) часто описываемым вариантам реконструкции (архитектура имплантата, концепция фиксации и маршрут материал/АП) в Рис. S5 (Дополнительные материалы) представлено концептуальное дерево принятия решений. Данная схема задумана как вспомогательное средство синтеза, а не как предписывающий клинический алгоритм.
В совокупности выявленные проблемы определяют чёткую трансляционную повестку: формирование более богатых, дефект-ориентированных клинических наборов данных; совместная оптимизация скаффолда, фиксации и реабилитации; систематическое исследование конструктивного пространства решётчатых структур и материалов; стандартизация моделирования и испытаний; и индустриализация рабочего процесса «от визуализации к имплантату». При согласовании этих элементов пациент-специфичные и модульные пористые конструкции хорошо позиционированы для того, чтобы стать рутинным вариантом лечения сегментарных дефектов бедренной и большеберцовой костей, а не нишевым решением для исключительных случаев.
9. Заключение и перспективы
Настоящий обзор показывает, как CT-основанная, пациент-специфичная реконструкция с архитектурированными пористыми имплантатами меняет подходы к лечению крупных сегментарных дефектов длинных трубчатых костей. При совокупном рассмотрении имеющихся исследований — от чисто расчётных работ через стендовые механические и биологические испытания, доклинические модели на животных и ранние клинические серии — прослеживается общая закономерность: успешная реконструкция определяется не наличием единственного «идеального» скаффолда, а достижением согласованного соответствия между архетипом дефекта, стратегией фиксации, архитектурой решётчатой структуры и биологией хозяина. При достижении такого соответствия пористые металлические и полимерно-керамические конструкции могут обеспечить стабильную передачу нагрузки, пространство для регенерации кости и восстановление оси конечности в ситуациях, которые прежде нередко приводили к ампутации или высокоморбидным реконструктивным вмешательствам.
Вместе с тем данная область ограничена разрозненной отчётностью и недостаточной детализацией геометрии дефекта, конфигурации фиксации, условий нагружения и результатов заживления. По 27 включённым исследованиям моделирование и механические испытания доминируют (70% и 56% соответственно), тогда как in vivo биологические конечные точки отражены лишь в 33%, что подчёркивает устойчивый «валидационный разрыв», ограничивающий клиническую трансляцию. Преодоление этого разрыва потребует трёх взаимодополняющих направлений: дефект-ориентированных наборов данных, последовательно фиксирующих анатомические, механические, биологические и долгосрочные результаты; конструктивных алгоритмов, явно связывающих архитектуру скаффолда и фиксацию с механической средой заживления; и надёжных, стандартизированных рабочих процессов «от визуализации к имплантату», включая обеспечение качества и валидацию как расчётных, так и экспериментальных данных. Если эти элементы удастся интегрировать и шире распространить, пациент-специфичные пористые реконструкции имеют потенциал для перехода от единичных клинических отчётов к воспроизводимым, стандартизированным клиническим рабочим процессам для сегментарных дефектов бедренной и большеберцовой костей.
Литература
- MarraraG. ZampognaB. SchickV.D. LarizzaL. RizzoP. SanzarelloI. NanniM. LeonettiD. Post-Traumatic Segmental Tibial Defects Management: A Systematic Review of the LiteratureAppl. Sci.2024156410.3390/app15010064
- WangQ. MaT. LiZ. ZhangK. HuangQ. Semi-focal bone transport versus traditional bone transport technique for the management of large tibial bone defects after traumaSci. Rep.202414798210.1038/s41598-024-58548-z38575734PMC10994901
- LuY. LaiC.Y. LaiP.J. YuY.H. Induced Membrane Technique for the Management of Segmental Femoral Defects: A Systematic Review and Meta-Analysis of Individual Participant DataOrthop. Surg.202315283710.1111/os.1360436444955PMC9837298
- SchickV.D. ZampognaB. MarraraG. SiracusanoL. LarizzaL. CalaciuraS. SanzarelloI. MarinozziA. LeonettiD. Custom-Made 3D-Printed Titanium Implants for Managing Segmental Distal Tibial Bone Defects: A Systematic Literature ReviewJ. Clin. Med.202514179610.3390/jcm1406179640142604PMC11943216
- McAnenaA.P. McClennenT. ZhengH. Patient-specific 3-dimensional-printed orthopedic implants and surgical devices are potential alternatives to conventional technology but require additional characterizationClin. Orthop. Surg.202417110.4055/cios2329439912074PMC11791502
- LiZ. LuM. ZhangY. WangJ. WangY. GongT. HeX. LuoY. ZhouY. MinL. 3D-Printed personalized lattice implant as an innovative strategy to reconstruct geographic defects in load-bearing bonesOrthop. Surg.20241682182910.1111/os.1400338296795PMC10984818
- MaJ. LiY. MiY. GongQ. ZhangP. MengB. WangJ. WangJ. FanY. Novel 3D printed TPMS scaffolds: Microstructure, characteristics and applications in bone regenerationJ. Tissue Eng.2024152041731424126368910.1177/2041731424126368939071895PMC11283664
- WakjiraY. CioniA. LemuH.G. Current status of the application of additive-manufactured TPMS structure in bone tissue engineeringProg. Addit. Manuf.2025101085110210.1007/s40964-024-00714-w
- TauheedM. AlsheghriA. DalaqA.S. Al-RubR.K.A. Bone-inspired lattice structures for biomedical applications: Design, pore network analysis, and mechanical performanceResults Eng.20252710569710.1016/j.rineng.2025.105697
- GandhiR. SalmiM. RoyB. PagliariL. ConcliF. Mechanical performance, fatigue behaviour, and biointegration of additively manufactured architected latticesVirtual Phys. Prototyp.202520e253073310.1080/17452759.2025.2530733
- AlkentarR. KladovasilakisN. TzetzisD. MankovitsT. Effects of pore size parameters of titanium additively manufactured lattice structures on the osseointegration process in orthopedic applications: A comprehensive reviewCrystals20231311310.3390/cryst13010113
- PoelertS. ValstarE. WeinansH. ZadpoorA.A. Patient-specific finite element modeling of bonesProc. Inst. Mech. Eng. Part H J. Eng. Med.201322746447810.1177/095441191246788423637222
- TaylorM. BryanR. GallowayF. Accounting for patient variability in finite element analysis of the intact and implanted hip and knee: A reviewInt. J. Numer. Methods Biomed. Eng.20132927329210.1002/cnm.253023255372
- WuP.K. TsaiW.C. WangH.W. LinC.L. Establishment of design guidelines for patient-specific 3D-printed reconstruction implants for large distal femoral defectsMater. Des.202525111366810.1016/j.matdes.2025.113668
- NamvarA. LozanovskiB. DowningD. WilliamsonT. KastratiE. ShididD. HillD. BuehnerU. RyanS. ChoongP.F. Finite element analysis of patient-specific additive-manufactured implantsFront. Bioeng. Biotechnol.202412138681610.3389/fbioe.2024.138681638784769PMC11111884
- LaubachM. CheersG.M. Frankenbach-DésorT. WeimerL.P. BaumgartnerH. BöckerW. BurgkartR. CidonioG. D’EsteM. DirnaglU. Clinical translation of 3D-printed patient-specific bone implants: A consensus statementInt. J. Surg.20251117497750610.1097/JS9.000000000000294440697079PMC12626479
- TetsworthK. WoloszykA. GlattV. 3D printed titanium cages combined with the Masquelet technique for the reconstruction of segmental femoral defects: Preliminary clinical results and molecular analysis of the biological activity of human-induced membranesOTA Int.20192e01610.1097/OI9.000000000000001633937652PMC7953522
- Blázquez-CarmonaP. Mora-MacíasJ. Martínez-VázquezF.J. MorgazJ. DomínguezJ. Reina-RomoE. Mechanics predicts effective critical-size bone regeneration using 3d-printed bioceramic scaffoldsTissue Eng. Regen. Med.20232089390410.1007/s13770-023-00577-237606809PMC10519928
- GoldsteinR.Y. JordanC.J. McLaurinT.M. GrantA. The Evolution of the Ilizarov TechniqueBull. Hosp. Jt. Dis.201371899524032588
- GautierE. SommerC. Guidelines for the clinical application of the LCPInjury200334637610.1016/j.injury.2003.09.02614580987
- ShamsM. MansurovZ. DaulbayevC. BakbolatB. Effect of Lattice Structure and Composite Precursor on Mechanical Properties of 3D-Printed Bone ScaffoldsEurasian-Chem.-Technol. J.20212325726610.18321/ectj1129
- JinH. ZhuoY. SunY. FuH. HanZ. Microstructure design and degradation performance in vitro of three-dimensional printed bioscaffold for bone tissue engineeringAdv. Mech. Eng.201911168781401988378410.1177/1687814019883784
- VermaR. KumarJ. SinghN.K. RaiS.K. SaxenaK.K. XuJ. Design and analysis of biomedical scaffolds using TPMS-based porous structures inspired from additive manufacturingCoatings20221283910.3390/coatings12060839
- LiuL. LiuC. DengC. WangX. LiuX. LuoM. WangS. LiuJ. Design and performance analysis of 3D-printed stiffness gradient femoral scaffoldJ. Orthop. Surg. Res.20231812010.1186/s13018-023-03612-z36804017PMC9938570
- DavoodiE. MontazerianH. MirhakimiA.S. ZhianmaneshM. IbhadodeO. ShahabadS.I. EsmaeilizadehR. SarikhaniE. ToorandazS. SarabiS.A. Additively manufactured metallic biomaterialsBioact. Mater.20221521424910.1016/j.bioactmat.2021.12.02735386359PMC8941217
- WuP.K. LeeC.W. SunW.H. LinC.L. Biomechanical analysis and design method for patient-specific reconstructive implants for large bone defects of the distal lateral femurBiosensors202112410.3390/bios1201000435049632PMC8773582
- ChangC.M. WongP.C. OuS.L. KoC.E. WangY.T. Optimizing implant lattice design for large distal femur defects: Stimulating interface bone growth to enhance osseointegrationInt. J. Bioprinting202410259010.36922/ijb.2590
- FindeisenS. SchwilkM. HaubruckP. FerbertT. HelbigL. MiskaM. SchmidmaierG. TannerM.C. Matched-Pair Analysis: Large-Sized Defects in Surgery of Lower Limb NonunionsJ. Clin. Med.202312423910.3390/jcm1213423937445272PMC10342412
- MaX.Y. YuanH. CuiD. LiuB. HanT.Y. YuH.L. ZhouD.P. Management of segmental defects post open distal femur fracture using a titanium cage combined with the Masquelet technique A single-centre report of 23 casesInjury20235411113010.1016/j.injury.2023.11113037890289
- CaoZ.m. SuiX.l. XiaoY. QingL.m. WuP.f. TangJ.y. Efficacy comparison of vascularized iliac crest bone flap and Ilizarov bone transport in the treatment of traumatic bone defects of the tibia combined with large soft tissue defectsJ. Orthop. Surg. Res.20231834910.1186/s13018-023-03783-937170110PMC10176677
- DheenadhayalanJ. ImranA. DevendraA. VenkatramaniH. VelmurugesanP.S. RajasekaranS. SabapathyS.R. Can locking plate fixation and free Vascularised fibular transfer with skin island achieve good functional outcome in the treatment of large bone defects of Tibia? A study of 26 casesInjury20245511146510.1016/j.injury.2024.11146538508984
- FengD. ZhangY. WuW. JiaH. MaC. Docking site complications analysis of Ilizarov bone transport technique in the treatment of tibial bone defectsJ. Orthop. Surg. Res.20231888910.1186/s13018-023-04356-637993906PMC10666420
- VahabiA. KayaH. KerekulovB. BiçerA. KeçeciB. SabahD. Does Augmenting Irradiated Autografts With Free Vascularized Fibula Graft in Patients With Bone Loss From a Malignant Tumor Achieve Union, Function, and Complication Rate Comparably to Patients Without Bone Loss and Augmentation When Reconstructing Intercalary Resections in the Lower Extremity?Clin. Orthop. Relat. Res.20254831680169510.1097/corr.000000000000359940569278PMC12373105
- SonW.S. LimE.J. KimB.S. ChoiW. ChoJ.W. OhJ.K. Consolidation of the Anteromedial Aspect of the Tibia Is Inferior to the Other Areas in the Reconstruction of Critical-Sized Bone Defect of the Tibial Shaft Using the Induced Membrane Technique: An Analysis of 111 Serial Computed Tomography of 37 PatientsJ. Orthop. Trauma202539465610.1097/BOT.000000000000292839787507
- LiuK. ZhangH. MaimaitiX. YusufuA. Bifocal versus trifocal bone transport for the management of tibial bone defects caused by fracture-related infection: A meta-analysisJ. Orthop. Surg. Res.20231814010.1186/s13018-023-03636-536841800PMC9968413
- HuangQ. MaT. XuY. LuY. LiM. WangQ. RenC. XueH. LiZ. ZhangK. Acute shortening and double-level lengthening versus bone transport for the management of large tibial bone defects after trauma and infectionInjury20235498399010.1016/j.injury.2023.01.02936658026
- PapakostidisC. GiannoudisP.V. Reconstruction of infected long bone defects: Issues and ChallengesInjury202354 380781010.1016/j.injury.2023.01.05236828614
- MiglioriniF. PadulaG.L. TorsielloE. SpieziaF. OlivaF. MaffulliN. Strategies for large bone defect reconstruction after trauma, infections or tumour excision: A comprehensive review of the literatureEur. J. Med. Res.20212611810.1186/s40001-021-00593-934600573PMC8487570
- ToogoodP. MiclauT. Critical-Sized Bone Defects: Sequence and PlanningJ. Orthop. Trauma201731S23S2610.1097/BOT.0000000000000980PMC567899228938387
- CoronaP.S. RosellC.C. VicenteM. SerracantaJ. TetsworthK. Three-stage limb salvage in tibial fracture related infection with composite bone and soft-tissue defectArch. Orthop. Trauma Surg.20221423877388710.1007/s00402-021-04299-934936017PMC9596551
- ZollerS.D. CaoL.A. SmithR.A. SheppardW. LordE.L. HamadC.D. GhodasraJ.H. LeeC. JeffcoatD. Staged reconstruction of diaphyseal fractures with segmental defects: Surgical and patient-reported outcomesInjury2017482248225210.1016/j.injury.2017.06.01828712488
- MasqueletA.C. KishiT. BenkoP.E. Very long-term results of post-traumatic bone defect reconstruction by the induced membrane techniqueOrthop. Traumatol. Surg. Res.201910515916610.1016/j.otsr.2018.11.01230639175
- MolinaC.S. StinnerD.J. ObremskeyW.T. Treatment of Traumatic Segmental Long-Bone Defects: A Critical Analysis ReviewJBJS Rev.20142e110.2106/JBJS.RVW.M.0006227490871
- ChenZ. XingY. LiX. LiuB. LiuN. HuoY. TianY. 3D-printed titanium porous prosthesis combined with the Masquelet technique for the management of large femoral bone defect caused by osteomyelitisBMC Musculoskelet. Disord.20242547410.1186/s12891-024-07576-x38880911PMC11181595
- TetsworthK. BlockS. GlattV. Putting 3D modelling and 3D printing into practice: Virtual surgery and preoperative planning to reconstruct complex post-traumatic skeletal deformities and defectsSICOT-J201731610.1051/sicotj/201604328220752PMC5319375
- OllivierM. BulaïdY. JacquetC. PesentiS. ArgensonJ.n. ParratteS. Fixation augmentation using calcium-phosphate bone substitute improves outcomes of complex tibial plateau fractures. A matched, cohort studyInt. Orthop.2018422915292310.1007/s00264-018-3926-729627848
- LefaivreK.A. SlobogeanG. O’HaraN.N. O’BrienP.J. Far Cortical Locking Versus Standard Constructs for Locked Plate Fixation in the Treatment of Acute, Displaced Fractures of the Distal FemurJ. Bone Jt. Surg.20241061739174910.2106/JBJS.23.0139039853223
- RoddyE. DavisK. WilsonP. KlewenoC. DunbarR.P. BareiD. Outcomes of Nonunion Repair for Distal Femur FractureJ. Orthop. Trauma20253962162810.1097/BOT.000000000000304740709936
- FowlerT. WhitehouseM. RiddickA. KhanU. KellyM. A Retrospective Comparative Cohort Study Comparing Temporary Internal Fixation to External Fixation at the First Stage Debridement in the Treatment of Type IIIB Open Diaphyseal Tibial FracturesJ. Orthop. Trauma20193312513010.1097/BOT.000000000000136230779724
- ZaheerM.U. RazzaqM.H. AycanM.F. MishraY.K. AI-Assisted Design and Evaluation of SLM-Ti64 Implants for Enhanced Bone RegenerationAdv. Healthc. Mater.202514e0315410.1002/adhm.20250315440906356PMC12716229
- WhitlockK.G. BrodkeD.J. KhouryP.H. LiV. BellA. OkhuereigbeD. SciadiniM.F. NasconeJ.W. O’TooleR.V. O’HaraN.N. Ring Fixator Bone Transport Is Associated With Fewer Unplanned Major Reoperations Than Masquelet in the Treatment of Segmental Bone Defects of the TibiaJ. Orthop. Trauma20253916116610.1097/BOT.000000000000295339750033
- WuW. ZhaoZ. WangY. YaoB. ShiP. LiuM. PengB. Clinical observation and finite element analysis of femoral stable interlocking intramedullary nail in intertrochanteric fracturesInt. Orthop.2023472319232610.1007/s00264-023-05865-z37358574
- WongK.W. WuC.D. ChienC.S. LeeC.W. YangT.H. LinC.L. Patient-specific 3-dimensional printing titanium implant biomechanical evaluation for complex distal femoral open fracture reconstruction with segmental large bone defect: A nonlinear finite element analysisAppl. Sci.202010409810.3390/app10124098
- KaruppudaiyanS. SinghD.K.J. SantoshV.M. Finite element analysis of scaffold for large defect in femur boneIOP Conf. Ser. Mater. Sci. Eng.201840201209610.1088/1757-899X/402/1/012096
- EntezariA. ZhangZ. SueA. SunG. HuoX. ChangC.C. ZhouS. SwainM.V. LiQ. Nondestructive characterization of bone tissue scaffolds for clinical scenariosJ. Mech. Behav. Biomed. Mater.20198915016110.1016/j.jmbbm.2018.08.03430286374
- RanaM. ChaudhuriA. BiswasJ.K. KarimS.I. DattaP. KarmakarS.K. RoychowdhuryA. Design of patient specific bone stiffness mimicking scaffoldProc. Inst. Mech. Eng. Part H J. Eng. Med.20212351453146210.1177/0954411921103071534227419
- ZhangT. WeiQ. ZhouH. JingZ. LiuX. ZhengY. CaiH. WeiF. JiangL. YuM. Three-dimensional-printed individualized porous implants: A new “implant-bone” interface fusion concept for large bone defect treatmentBioact. Mater.202163659367010.1016/j.bioactmat.2021.03.03033898870PMC8056181
- PoblothA.M. ChecaS. RaziH. PetersenA. WeaverJ.C. Schmidt-BleekK. WindolfM. TataiA.Á. RothC.P. SchaserK.D. Mechanobiologically optimized 3D titanium-mesh scaffolds enhance bone regeneration in critical segmental defects in sheepSci. Transl. Med.201810eaam882810.1126/scitranslmed.aam882829321260
- ObatonA.F. FainJ. MeinelD. TsamosA. LéonardF. LécuelleB. DjemaïM. In vivo bone progression in and around lattice implants additively manufactured with a new titanium alloyAppl. Sci.202313728210.3390/app13127282
- KaruppudaiyanS. SinghD.K.J. Design of scaffold with controlled internal architecture using fused deposition modeling (FDM)Int. J. Eng. Adv. Technol.201992764276810.35940/ijeat.A9769.109119
- YavariS.A. van der StokJ. AhmadiS. WauthléR. SchrootenJ. WeinansH. ZadpoorA.A. Mechanical analysis of a rodent segmental bone defect model: The effects of internal fixation and implant stiffness on load transferJ. Biomech.2014472700270810.1016/j.jbiomech.2014.05.00624882739
- LeeS.S. DuX. SmitT. BissaccoE.G. SeilerD. de WildM. FergusonS.J. 3D-printed LEGO®-inspired titanium scaffolds for patient-specific regenerative medicineBiomater. Adv.202315421361710.1016/j.bioadv.2023.21361737678088
- VasanthanathanA. KennedyS.M. Bio-printing of femur model: A bone substitute for biomedical researchMater. Technol.20235728328910.17222/mit.2023.831
- GabarreS. AlbaredaJ. GraciaL. PuértolasS. IbarzE. HerreraA. Influence of gap size, screw configuration, and nail materials in the stability of anterograde reamed intramedullary nail in femoral transverse fracturesInjury201748S40S4610.1016/S0020-1383(17)30793-329162240
- NoyamaY. NakanoT. IshimotoT. SakaiT. YoshikawaH. Design and optimization of the oriented groove on the hip implant surface to promote bone microstructure integrityBone20135265966710.1016/j.bone.2012.11.00523147000
- LuJ. GuoS.C. WangQ.Y. ShengJ.G. TaoS.C. J-bone graft with double locking plate: A symphony of mechanics and biology for atrophic distal femoral non-union with bone defectJ. Orthop. Surg. Res.20201514410.1186/s13018-020-01636-332293488PMC7161247
- BervenH. BrixM. IzadpanahK. KuboschE.J. SchmalH. Comparing case-control study for treatment of proximal tibia fractures with a complete metaphyseal component in two centers with different distinct strategies: Fixation with Ilizarov frame or locking platesJ. Orthop. Surg. Res.20181312110.1186/s13018-018-0792-329788992PMC5964904
- ArabnejadS. JohnstonB. TanzerM. PasiniD. Fully porous 3D printed titanium femoral stem to reduce stress-shielding following total hip arthroplastyJ. Orthop. Res.2017351774178310.1002/jor.2344527664796
- YamakoG. JanssenD. HanadaS. AnijsT. OchiaiK. TotoribeK. ChosaE. VerdonschotN. Improving stress shielding following total hip arthroplasty by using a femoral stem made of β type Ti-33.6Nb-4Sn with a Young’s modulus gradationJ. Biomech.20176313514310.1016/j.jbiomech.2017.08.01728882332
- GlassmanA.H. BobynJ.D. TanzerM. New femoral designs: Do they influence stress shielding?Clin. Orthop. Relat. Res.2006453647410.1097/01.blo.0000246541.41951.2117312586
- Shayesteh MoghaddamN. Taheri AndaniM. Metals for bone implants: Safety, design, and efficacyBiomanufacturing Rev.20161110.1007/s40898-016-0001-2
- ZhangQ.H. CosseyA. TongJ. Stress shielding in periprosthetic bone following a total knee replacement: Effects of implant material, design and alignmentMed. Eng. Phys.2016381481149010.1016/j.medengphy.2016.09.01827745873
- ChmielewskaA. DeanD. The role of stiffness-matching in avoiding stress shielding-induced bone loss and stress concentration-induced skeletal reconstruction device failureActa Biomater.2024173516510.1016/j.actbio.2023.11.01137972883
- CeddiaM. MorizioA. SolarinoG. TrentadueB. Evaluation of the Stress-Shielding Effect of a PEEK Knee Prosthesis: A Finite Element StudyOsteology202552410.3390/osteology5030024
- GraulichT. KranzC. KorallusC. ÖrgelM. HaertléM. OmarM. KrettekC. PanzicaM. Patients outcome after distal femur- and proximal tibia replacementOrthop. J. Sport. Med.202082325967120S003210.1177/2325967120S00322
- MatarH.E. BlochB.V. JamesP.J. Distal Femoral Replacements for Acute Comminuted Periprosthetic Knee Fractures: Satisfactory Clinical Outcomes at Medium-Term Follow-upArthroplast. Today20217374210.1016/j.artd.2020.11.01433521195PMC7818597
- McAleeseT. McLeodA. KeoghC. HartyJ.A. Mechanical outcomes of the TFNA, InterTAN and IMHS intramedullary nailing systems for the fixation of proximal femur fracturesInjury20245511118510.1016/j.injury.2023.11118538070327
- StadelmannV. Prevention of Micromotion-Related Periprosthetic Bone Loss Using Local Release of Bisphosphonate: Theoretical Developments and Experimental ValidationsPh.D. ThesisEPFL—Swiss Federal Technology Institute of LausanneLausanne, Switzerland2008
- SopherR.S. AmisA.A. JeffersJ.R.T. Total ankle replacement design and positioning affect implant-bone micromotion and bone strainsMed. Eng. Phys.201747475510.1016/j.medengphy.2017.01.02228233732PMC5360194
- KlasanA. MagillP. FramptonC. ZhuM. YoungS.W. Factors predicting repeat revision and outcome after aseptic revision total knee arthroplasty: Results from the New Zealand Joint RegistryKnee Surg. Sport. Traumatol. Arthrosc.20202957958510.1007/s00167-020-05985-832279110
- NolteP.C. SchlentrichK. RaischP. JungM.K. GrütznerP.A. BischelO. Survival and Clinical Outcomes after Unconstrained Total Knee Arthroplasty for Tibial Plateau Fractures–A Retrospective Study with Minimum 4-Year Follow-UpJ. Clin. Med.202312730310.3390/jcm1223730338068355PMC10706982
- RissolioL. SabatiniL. RisitanoS. BistolfiA. GalluzzoU. MassèA. IndelliP.F. Is It the Surgeon, the Patient, or the Device? A Comprehensive Clinical and Radiological Evaluation of Factors Influencing Patient Satisfaction in 648 Total Knee ArthroplastiesJ. Clin. Med.202110259910.3390/jcm1012259934204628PMC8231230
- WeisS. SeifertL. OltmannsM. KhuryF. BiegerR. FaschingbauerM. The Etiology of Total Knee Arthroplasty Failure Influences on Improvement in Knee Function: A Follow-Up StudyJ. Clin. Med.202413767210.3390/jcm1324767239768594PMC11677656
- WiedingJ. SouffrantR. MittelmeierW. BaderR. Finite element analysis on the biomechanical stability of open porous titanium scaffolds for large segmental bone defects under physiological load conditionsMed. Eng. Phys.20133542243210.1016/j.medengphy.2012.06.00622809675
- BayogluR. OkyarA.F. Implementation of boundary conditions in modeling the femur is critical for the evaluation of distal intramedullary nailingMed. Eng. Phys.2015371053106010.1016/j.medengphy.2015.08.00626341599
- CharbonnierB. ManasseroM. BourguignonM. DecambronA. El-HafciH. MorinC. LeonD. BensidoumM. CorsiaS. PetiteH. Custom-made macroporous bioceramic implants based on triply-periodic minimal surfaces for bone defects in load-bearing sitesActa Biomater.202010925426610.1016/j.actbio.2020.03.01632194263
- KellyC.N. LinA.S. LeguinecheK.E. ShekharS. WalshW.R. GuldbergR.E. GallK. Functional repair of critically sized femoral defects treated with bioinspired titanium gyroid-sheet scaffoldsJ. Mech. Behav. Biomed. Mater.202111610438010.1016/j.jmbbm.2021.10438033588248
- LeeM.C. PanC.T. ChenW.F. LinM.C. ShiueY.L. Design, manufacture, and characterization of a critical-sized gradient porosity dual-material tibial defect scaffoldBioengineering20241130810.3390/bioengineering1104030838671730PMC11047886
- AcarA.A. DaskalakisE. BartoloP. WeightmanA. CooperG. BlunnG. KocB. Customized scaffolds for large bone defects using 3D-printed modular blocks from 2D-medical imagesBio-Des. Manuf.20247748710.1007/s42242-023-00259-x
- LuH.T. HsuC.C. JianQ.Q. ChenW.T. Biomechanical Study of Different Scaffold Designs for Reconstructing a Traumatic Distal Femur Defect Using Patient-Specific Computational ModelingComput. Model. Eng. Sci. (CMES)20251421883189810.32604/cmes.2025.057675
- BenadyA. MeyerS.J. GoldenE. DadiaS. LevyG.K. Patient-specific Ti-6Al-4V lattice implants for critical-sized load-bearing bone defects reconstructionMater. Des.202322611160510.1016/j.matdes.2023.111605
- BavilA. Eghan-AcquahE. DiamondL. BarrettR. CartyC. BarzanM. NasseriA. LloydD. SaxbyD. FeihS. Effect of different constraining boundary conditions on simulated femoral stresses and strains during gaitSci. Rep.2024141080810.1038/s41598-024-61305-x38734763PMC11088641
- ScheinerS. HellmichC. Patient-specific design of tissue engineering scaffolds, based on mathematical modelingAdvances in Ceramic BiomaterialsWoodhead PublishingCambridge, UK2017391406
- LaubachM. HildebrandF. SureshS. WagelsM. KobbeP. GilbertF. KneserU. HolzapfelB.M. HutmacherD.W. The concept of scaffold-guided bone regeneration for the treatment of long bone defects: Current clinical application and future perspectiveJ. Funct. Biomater.20231434110.3390/jfb1407034137504836PMC10381286
- PankajP. Patient-specific modelling of bone and bone-implant systems: The challengesInt. J. Numer. Methods Biomed. Eng.20132923324910.1002/cnm.253023281281
- HahnH. PalichW. Preliminary evaluation of porous metal surfaced titanium for orthopedic implantsJ. Biomed. Mater. Res.1970457157710.1002/jbm.8200404075487557
- GalanteJ. RostokerW. Fiber metal composites in the fixation of skeletal prosthesisJ. Biomed. Mater. Res.19737436110.1002/jbm.8200703054717965
- SpectorM. Historical review of porous-coated implantsJ. Arthroplast.1987216317710.1016/S0883-5403(87)80024-43302108
- FabiD. LevineB. Porous coatings on metallic implant materialsMaterials for Medical DevicesASM InternationalMaterials Park, OH, USA2012307319
- EnghC.A. BobynJ.D. GlassmanA.H. Porous-coated hip replacement. The factors governing bone ingrowth, stress shielding, and clinical resultsJ. Bone Jt. Surg. Br.198769455510.1302/0301-620X.69B1.38187323818732
- EskolaA. VahvanenV. SantavirtaS. HonkanenV. SlätisP. Porous-coated anatomic (PCA) knee arthroplasty: 3-Year resultsJ. Arthroplast.1992722322810.1016/0883-5403(92)90040-W1402934
- NakoshiY. HasegawaM. SudoA. UchidaA. A long-term follow-up study of the cementless THA with anatomic stem/HGPII cup with 22-mm headInt. Orthop.20093338138510.1007/s00264-007-0505-818183396PMC2899065
- MowC.S. WiedelJ.D. Revision total knee arthroplasty using the porous-coated anatomic revision prosthesis: Six-to twelve-year resultsJ. Arthroplast.19981368168610.1016/S0883-5403(98)80013-29741446
- RezapourianM. JasiukI. SaarnaM. HussainovaI. Selective laser melted Ti6Al4V split-P TPMS lattices for bone tissue engineeringInt. J. Mech. Sci.202325110835310.1016/j.ijmecsci.2023.108353
- GuoX. DingJ. LiX. QuS. SongX. FuhJ.Y.H. LuW.F. ZhaiW. Enhancement in the mechanical behaviour of a Schwarz Primitive periodic minimal surface lattice structure designInt. J. Mech. Sci.202221610697710.1016/j.ijmecsci.2021.106977
- LiY. JiangD. ZhaoR. WangX. WangL. ZhangL.C. High mechanical performance of lattice structures fabricated by additive manufacturingMetals202414116510.3390/met14101165
- BenedettiM. Du PlessisA. RitchieR.O. DallagoM. RazaviN. BertoF. Architected cellular materials: A review on their mechanical properties towards fatigue-tolerant design and fabricationMater. Sci. Eng. R Rep.202114410060610.1016/j.mser.2021.100606
- RezapourianM. KambojN. JasiukI. HussainovaI. Biomimetic design of implants for long bone critical-sized defectsJ. Mech. Behav. Biomed. Mater.202213410537010.1016/j.jmbbm.2022.10537035872461
- Sahafnejad-MohammadiI. RahmatiS. NajmoddinN. BodaghiM. Biomimetic polycaprolactone-graphene oxide composites for 3D printing bone scaffoldsMacromol. Mater. Eng.2023308220055810.1002/mame.202200558
- MallA.P. BhandarkarV.V. MandaloiG. TandonP. An overview of design and development of biomimetic bone scaffolds using heterogeneous TPMS lattice structuresArch. Comput. Methods Eng.2024322429245610.1007/s11831-024-10212-5
- RezapourianM. HussainovaI. Optimal mechanical properties of Hydroxyapatite gradient Voronoi porous scaffolds for bone applications—A numerical studyJ. Mech. Behav. Biomed. Mater.202314810623210.1016/j.jmbbm.2023.10623237952505
- QuH. HanZ. ChenZ. TangL. GaoC. LiuK. PanH. FuH. RuanC. Fractal design boosts extrusion-based 3D printing of bone-mimicking radial-gradient scaffoldsResearch20212021989268910.34133/2021/989268934909694PMC8637129
- FengP. LiuL. YangF. MinR. WuP. ShuaiC. Shape/properties collaborative intelligent manufacturing of artificial bone scaffold: Structural design and additive manufacturing processBiofabrication20241701200510.1088/1758-5090/ad905f39514965
- RezapourianM. Cheloee DarabiA. KhoshbinM. HussainovaI. Multi-Objective Machine Learning Optimization of Cylindrical TPMS Lattices for Bone ImplantsBiomimetics20251047510.3390/biomimetics1007047540710288PMC12292215
- MaskeryI. SturmL. AremuA.O. PanesarA. WilliamsC.B. TuckC.J. WildmanR.D. AshcroftI.A. HagueR.J. Insights into the mechanical properties of several triply periodic minimal surface lattice structures made by polymer additive manufacturingPolymer2018152627110.1016/j.polymer.2017.11.049
- KadkhodapourJ. SchmauderS. SajadiF. Quality Analysis of Additively Manufactured Metals: Simulation Approaches, Processes, and Microstructure PropertiesElsevierAmsterdam, The Netherlands2022
- RezapourianM. HussainovaI. Mechanical analysis of multi-surface TPMS lattices for bone applicationsProc. Est. Acad. Sci.20257422222710.3176/proc.2025.2.25
- LuY. ChengL. YangZ. LiJ. ZhuH. Relationship between the morphological, mechanical and permeability properties of porous bone scaffolds and the underlying microstructurePLoS ONE202015e023847110.1371/journal.pone.023847132870933PMC7462274
- TimercanA. SheremetyevV. BrailovskiV. Mechanical properties and fluid permeability of gyroid and diamond lattice structures for intervertebral devices: Functional requirements and comparative analysisSci. Technol. Adv. Mater.20212228530010.1080/14686996.2021.190722233967629PMC8079052
- ToosiS. Javid-NaderiM.J. TamayolA. EbrahimzadehM.H. YaghoubianS. Mousavi ShaeghS.A. Additively manufactured porous scaffolds by design for treatment of bone defectsFront. Bioeng. Biotechnol.202411125263610.3389/fbioe.2023.125263638312510PMC10834686
- sadat MirhakimiA. DubeyD. ElbestawiM.A. Laser powder bed fusion of bio-inspired metamaterials for energy absorption applications: A reviewJ. Mater. Res. Technol.2024312126215510.1016/j.jmrt.2024.06.234
- CastrisosG. MatheusI.G. SparksD. LoweM. WardN. SehuM. WilleM.L. PhuaY. SaviF.M. HutmacherD. Regenerative matching axial vascularisation of absorbable 3D-printed scaffold for large bone defects: A first in human seriesJ. Plast. Reconstr. Aesthetic Surg.2022752108211810.1016/j.bjps.2022.02.05735370116
- SparksD.S. SaviF.M. DlaskaC.E. SaifzadehS. BrierleyG. RenE. CipitriaA. ReichertJ.C. WilleM.L. SchuetzM.A. Convergence of scaffold-guided bone regeneration principles and microvascular tissue transfer surgerySci. Adv.20239eadd607110.1126/sciadv.add607137146134PMC10162672
- SparksD.S. WiperJ. LloydT. WilleM.L. SehuM. SaviF.M. WardN. HutmacherD.W. WagelsM. Protocol for the BONE-RECON trial: A single-arm feasibility trial for critical sized lower limb BONE defect RECONstruction using the mPCL-TCP scaffold system with autologous vascularised corticoperiosteal tissue transferBMJ Open202313e05644010.1136/bmjopen-2021-056440PMC1016352837137563
- HasanabadiM. AsgariH. AziziN. AghajaniH. MinasyanT. ToyserkaniE. Towards sustainable additive manufacturing: Enhanced productivity via numerical-experimental melt pool engineering in laser powder bed fusion of Ti-alloyJ. Mater. Res. Technol.2025384100411410.1016/j.jmrt.2025.08.251
- EnriqueP.D. MinasyanT. ToyserkaniE. Laser powder bed fusion of difficult-to-print γ Ni-based superalloys: A review of processing approaches, properties, and remaining challengesAddit. Manuf.202510610481110.1016/j.addma.2025.104811
- LiuL. MinasyanT. IvanovR. AydinyanS. HussainovaI. Selective laser melting of TiB2-Ti composite with high content of ceramic phaseCeram. Int.202046211282113510.1016/j.ceramint.2020.05.189
- KadkhodapourJ. MirhakimiA.S. MontazerianH. Structural defects and mechanical properties of additively manufactured partsQuality Analysis of Additively Manufactured MetalsElsevierAmsterdam, The Netherlands2023119172
- MinasyanT. HussainovaI. Laser powder-bed fusion of ceramic particulate reinforced aluminum alloys: A reviewMaterials202215246710.3390/ma1507246735407800PMC8999622